Созревание ооцитов внутри фолликулов с разной степенью развития микроциркуляторного русла
Метод интрафолликулярного культивирования ооцитов разработан в начале 70-х годов. Основной причиной разработки этого метода послужило то обстоятельство, что при извлечении ооцитов из фолликулов нарушаются связи между ооцитом и клетками фолликула. Это приводит к изменениям структуры ооплазмы и ее функций. Надо полагать, что для созревания ооцитов необходимо участие многих элементов фолликулов [4]. Неудивительно, что в последнее время для полноценного созревания изолированных ооцитов используют совместное культивирование с клетками фолликулов. Интрафолликулярное культивирование представляет большой интерес в научном плане, так как этот способ позволяет изучать закономерности процессов, происходящих в фолликуле [15]. Целью настоящей работы являлось изучение изменений структур интактных и атретических фолликулов до и в процессе их культивирования, а также способности к оплодотворению яйцеклеток, созревших внутри фолликула, и дальнейшему развитию эмбрионов.
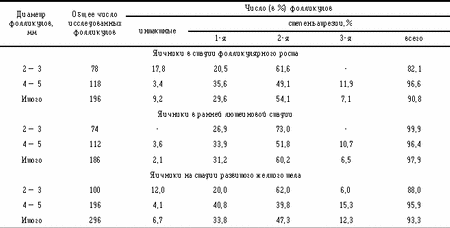
Материал и методыВыделение и оценка фолликуловАнтральные фолликулы диаметром 2 — 5 мм выделяли из яичников коров в разных стадиях полового цикла. При этом фолликулы со слабым тургором, “белесые”, “серые”, с темными пятнами в опытах не использовали. Выделенные фолликулы оценивали по состоянию и степени раз вития микроциркуляторного русла (МЦР) [1, 2]. Степень развития МЦР оценивали по 5-балльной системе. По исследуемым признакам популяция фолликулов была разделена на 4 группы: 1-я группа — фолликулы с обширной васкуляризацией, представленной плотной сетью капилляров без признаков дегенерации. Контуры сосудов ровные, без расширений, прерывистости (интактные фолликулы); 2-я группа — фолликулы с развитым МЦР, представленным более крупными микрососудами без признаков дегенерации (1-я степень атрезии); 3-я группа — фолликулы со слаборазвитым МЦР без признаков дегенерации, сеть капилляров отсутствовала (2-я степень атрезии); 4-я группа — фолликулы, МЦР которых имело признаки дегенерации (неровность контура, прерывистость сосудов) (3-я степень атрезии). Культивирование фолликуловКультивирование фолликулов проводили в роллерной установке в закрытых сосудах со специальной газовой смесью: 5% CO2, 55% O2, 40% N2. Время инкубации 6, 12, 18, 24, 30, 36, 42 ч. В качестве культуральной среды использовали Ham F-10 с добавлением FCS (20%), ФСГ (5 мкг/мл), ЛГ (5 мкг/мл), эстрадиола (1 мкг/мл), инсулина (1 мкг/мл). В результате предварительных исследований установлено, что в процессе культивирования фолликулов 1-й и 2-й групп между ними не существует выраженных морфологических и цитологических различий, поэтому фолликулы этих групп были объединены. Фолликулы 4-й группы для культивирования не использовались из-за глубоких деструктивных изменений всех их составных структур. Оплодотворение ооцитов, созревших внутри фолликуловЯйцеклетки, созревшие в фолликулах, выделяли и осеменяли капацитированными сперматозоидами быка. Продолжительность совместной инкубации яйцеклеток со сперматозоидами составляла 24 ч, после чего клетки переносили в свежеприготовленную среду. Первый просмотр клеток проводили через 28 ч после осеменения. При обнаружении признаков оплодотворения — наличие второго полярного тельца и борозды дробления — яйцеклетки инкубировали 24 — 78 ч. Гистологический и цитогенетический методыЧерез каждые 6 ч культивирования проводили гистологическое исследование фолликулов и готовили препараты мейотических хромосом. Фолликулы фиксировали в растворе Буэна, Карнуа. Заливку осуществляли через парафин. Срезы толщиной 5 — 7 мкм, проходящие через ядро ооцита, окрашивали гематоксилином по Эрлиху или Бемеру [16]. Препараты мейотических хромосом ооцитов готовили по методу Тарковского и окрашивали раствором Гимзы. Статистическую обработку полученных результатов проводили с применением критерия Стьюдента и критерия х2. РезультатыДля гистологического анализа было использовано 80 интактных фолликулов, по 20 фолликулов в каждой группе. Результаты гистологического анализа показали, что степень развития и состояние МЦР фолликулов коррелируют с состоянием всех клеточных структур фолликулов [1, 2, 5]. Фолликулы исследовали в зависимости от цикла яичника, степени развития и состояния МЦР (табл.1).
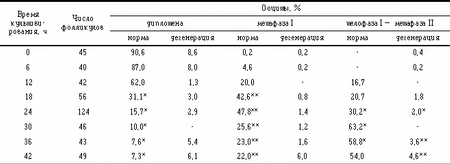
Как видно из табл.1, 82,1 — 99,9% фолликулов, выделенных из яичников разных стадий цикла, являлись атретическими, в том числе 90,8% на стадии фолликулярного роста, 97,9% на ранней лютеиновой стадии и 93,3% на стадии развитого желтого тела. Наибольшее число интактных фолликулов содержалось в яичниках на стадиях фолликулярного роста и развитого желтого тела (9,2 и 6,7%). Изучение состояния хроматина ооцитов, выделенных из фолликулов с различной степенью развития МЦР, показало, что в фолликулах с обширной васкуляризацией (1-я группа) ядерный материал ооцитов не имел признаков дегенерации. При уменьшении васкуляризации фолликулов 2-й и 3-й групп наблюдали возрастание числа ооцитов с признаками дегенерации хромосом (15,7 и 42,8% соответственно). Максимальное число (73,5%) таких ооцитов находилось в фолликулах с признаками дегенерации МЦР (4-я группа). Таким образом, результаты цитологического анализа ооцитов, выделенных из фолликулов с различной степенью развития МЦР, свидетельствуют, что фолликулы с обширной и развитой степенью васкуляризации (1-я и 2-я группы) имеют наименьшее число ооцитов с признаками дегенерации хромосом. Изучение динамики созревания интактных и 1-й степени атрезии интрафолликулярных ооцитов (1-я и 2-я группы) показало, что максимальное число ооцитов (47,8%) достигало стадии метафазы I без признаков дегенерации за 24 ч культивирования, а метафазы II — за 30 ч культивирования 63,2% (табл.2). На всех стадиях мейоза доля ооцитов с признаками дегенерации ядерного материала оставалась низкой.
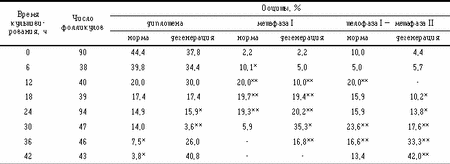
Примечание. Здесь и в табл.3 — 5 звездочками отмечены достоверные различия по отношению к контролю (время культивирования 0 ч): * — p(0,05, ** — p(0,001. При культивировании фолликулов 2-й степени атрезии (3-я группа) (табл.3) резко возрастало число ооцитов, имеющих хромосомы с признаками дегенерации (деконденсация, фрагментация, слипание) на всех стадиях мейоза. Таким образом, культивирование интактных фолликулов (1-я группа) и фолликулов 1-й степени атрезии (2-я группа) не сопровождается проявлениями атретических процессов, в то время как при культивировании фолликулов 2-й степени атрезии (3-я группа) наблюдается усиление признаков дегенерации хромосом на всех стадиях мейоза.
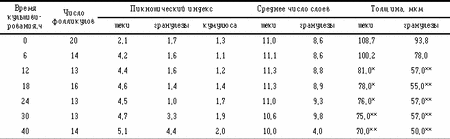
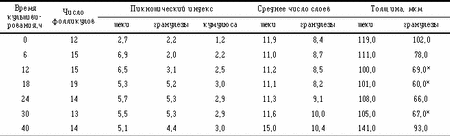
Примечание. Здесь и в табл. 5 * p(0,05; ** p=0,01. Морфогистологическое исследование фолликулов в процессе культивирования выявило, что в интактных фолликулах и фолликулах 1-й степени атрезии толщина теки достоверно уменьшалась (табл.4). Гранулеза хорошо развита. Среднее число слоев гранулезы составляло 8,6 — 9,8 и лишь при 40-часовом культивировании уменьшалось до 4 слоев. При культивировании фолликулов с 6 до 40 ч толщина гранулезы уменьшалась с 78 до 50 мкм за счет ее равномерной диссоциации. В процессе культивирования фолликулов 2-й степени атрезии (табл.5) клетки теки и гранулезы оказывались дезорганизованными. Пикнотический индекс гранулезы и кумулюса возрастал в среднем в 2 раза по сравнению с аналогичными показателями у интактных фолликулов и 1-й степени атрезии. Иногда клетки гранулезы отторгались в фолликулярную жидкость. В полости фолликула наблюдали множество дегенерированных клеток и пикнотических ядер.
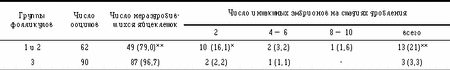
Таким образом, морфогистологический анализ фолликулов с разной степенью развития МЦР показал изменение клеточных структур фолликулов в процессе культивирования. При оплодотворении яйцеклеток, созревших в неатретических фолликулах и фолликулах 1-й степени атрезии (1-я и 2-я группы), развитие продолжалось до интактных эмбрионов (табл.6).
Примечание. В скобках — процент. Звездочками отмечена достоверность различия показателей 1-й и 2-й групп фолликулов в сравнении с 3-й группой; * — p(0,01, ** — p(0,001. Морфологический и цитологический анализ эмбрионов, полученных из оплодотворенных яйцеклеток, созревших в интактных фолликулах и фолликулах 1-й степени атрезии (1-я и 2-я группы), выявил, что бластомеры эмбрионов в основном были одинаковы по величине и форме и во всех бластомерах были ядра. При оплодотворении яйцеклеток, созревших в фолликулах со 2-й степенью атрезии (3-я группа), наблюдали неравномерное дробление, фрагментацию, частичный лизис. При исследовании таких эмбрионов не во всех бластомерах выявлялись ядра. Таким образом, из результатов нашей работы следует, что ооциты из интактных фолликулов и фолликулов 1-й степени атрезии в данных условиях культивирования способны к оплодотворению и дальнейшему развитию эмбрионов, а разработанный принцип разделения популяции фолликулов по состоянию МЦР позволяет прогнозировать не только состояние фолликулов, но и результаты созревания и оплодотворения. Обсуждение результатовВ литературе известны единичные работы, в которых оценка фолликулов мышей, овец и коров проводилась по состоянию МЦР [5, 7, 15]. Разработанная нами классификация позволила комплексно оценить состояние фолликулов до и в процессе культивирования. Вся популяция фолликулов была разделена на 4 группы. В качестве основного прижизненного морфологического признака полноценности фолликула использовано состояние МЦР: степень его развития, равномерность контуров сосудов, наличие или отсутствие прерывистости. Процесс атрезии антральных фолликулов многие исследователи разделяют на три последовательные стадии. Одним из важных показателей атретического процесса в тканях фолликулов служит появление пикнотических ядер. Вопрос о количестве пикнотических ядер в атретических фолликулах различными авторами решается неоднозначно [3, 7, 10, 12 — 17]. В нашей работе было показано, что по мере нарастания признаков атрезии увеличивается число пикнотических ядер в теке, гранулезе и кумулюсе. Самым устойчивым элементом фолликулов оказалась тека. Пикнотический индекс теки составил 7,0±0,76 в фолликулах 3-й степени атрезии. Такую высокую устойчивость теки можно объяснить, вероятно, наличием в этой ткани сосудов, выполняющих резорбтивную функцию. Нами было показано, что наиболее подверженной дегенерации в фолликулах является гранулеза. Причиной повышенной чувствительности клеток гранулезы служит, вероятно, отсутствие в ней сосудов, в результате чего происходит нарушение обменных и питательных функций этой ткани. В литературе известны многие исследования по установлению числа интактных и атретических фолликулов в яичнике [3, 7, 10, 11, 17]. Проведенный морфологический анализ фолликулов показал, что наибольшее число интактных фолликулов содержится в яичниках на стадиях фолликулярного роста и развитого желтого тела. В яичниках на ранней лютеиновой стадии фолликулы в основном атретические. В работе показано, что фолликулы коров обладают разной способностью к созреванию. Созревание ооцитов в интактных и 1-й степени атрезии фолликулах диаметром 2 — 5 мм происходит медленнее, чем созревание ооцитов в фолликулах 2-й степени атрезии. По-видимому, это связано с тем, что секреция клеток гранулезы в интактном фолликуле ингибирует созревание ооцита [6, 8, 9]. В атретических фолликулах значительная часть клеток, а иногда и вся гранулеза подвергается лизису. В результате этого ингибирующий эффект ослабевает и наступает реинициация мейоза. Культивирование фолликулов 2-й степени атрезии выявило значительное увеличение числа ооцитов с признаками дегенерации ядерного материала. Таким образом, разная степень атретических изменений, происходящих в клетках теки, гранулезы и кумулюса, оказывает влияние на состояние ооцита, в частности на способность к созреванию вне организма [10]. В наших экспериментах за 30 ч культивирования 63,2% ооцитов в интактных фолликулах и фолликулах 1-й степени атрезии (1-я и 2-я группы) и 23,6% ооцитов в фолликулах 2-й степени атрезии (3-я группа) созревали до стадии метафазы II. При этом признаки дегенерации хромосом у фолликулов 1-й и 2-й групп отсутствовали, а у фолликулов 3-й группы выявлены в 17,6% случаев. Таким образом, необходимо отметить, что в наших опытах в процессе культивирования наиболее существенные морфологические изменения происходили в гранулезе. Наименее выраженные изменения отмечены в теке. Клетки кумулюса занимали в этом отношении промежуточное положение. Атретические изменения, начавшиеся в гранулезе, а затем в кумулюсе и теке, затрагивают ооцит, что приводит к нарушению процесса оплодотворения яйцеклеток, полученных при созревании их в фолликулах со 2-й степенью атрезии. Литература1. Смирнова Т.А., Галиева Л.Д., Завертяев Б.П. и др. Цитоморфологическая оценка фолликулов коров. Пробл репрод 1995;2:23 — 25. 2. Смирнова Т.А., Галиева Л.Д., Свиридов Б.Е. Цитогенетический анализ ооцитов антральных фолликулов. Пробл репрод 1996;4:8 — 12. 3. Brand A., de Jong W.H.R. Qualitative and quantitative micromorphological investigations of the tertiary population during the oestrous cycle in sheep. J Reprod Fert 1973;33:431 — 439. 4. Campe del M.R., Campo del C.H., Mapletoft R.J., Ginter O.J. Morphology and location of atteched follicular cumulus-oocyte complexes in horses, cattle and llamas. Theriogenology 1995;43:533 — 542. 5. Driancourt M.A. Follicular dynamics in sheep and cattle. Theriogenology 1991;35:1:55 — 79. 6. Gouldiing D., Martin T.L., Williams D.H. et al. Effect of FSH on day 1 of the estrous cycle on follicule number and concentrations of inhibin in follicular fluid in heifers. Theriogenology 1991;36:65:1049 — 1057. 7. Hinrichs K. The relationship of follicle atresia to follicle size, oozyte recovery rate on aspiration, and oocyre morphology in the mare. Theriogenology 1991;36:2:157 — 168. 8. Hopko Ireland, Janet L., Ireland J.J. Changes in expression of inhibin/activin and subunit messenger ribonucleic acids following increases in size and during different stages of differentiation or atresia of non-ovulatory follicles in cows. Biol Reprod 1994;50:492 — 501. 9. Hopko Ireland, Janet L., Good T.E.M. et al. Alterations in amounts of different forms of inhibin during follicular atresia. Biol Reprod 1994;50:1265 — 1276. 10. Hurk van den R., Dijkstra G., Hulshof S.C.J., Vos P.L.A.M. Micromorphology of antral follicles in cattle after prostaglandin-induced luteolysis, with particular reference to atypical granulosa cells. J Reprod Fertil 1994;100:137 — 142. 11. Katska L., Smorang Z. Number and quality of oocytes in relation to age cattle. Anim Reprod Sci 1984;7:5:451 — 460. 12. Kruip Th.A.M., Dieleman S.J. Steroid hormone concentrations in the fluid of bovine follicles relative to size, guality and stage of the oestrus. Theriogenology 1985;24:4:395 — 408. 13. Kruip Th.A.M., Dieleman S.J. Intrinsinc and extrinsinc factors influencing steroid production in vitro by bovine follicles. Theriogenology 1989;31:3:531 — 544. 14. Leibfried-Rutledge M.L., Critser E.S., First N.L. Fertilization potencial of follicular oocytes classified by stage of cycle and size of follicle. Theriogenology 1985;23:5:753 — 760. 15. Moor R.M., Seamark R.F. Cell signaling permeability and microvasculatory changes during antrale follicle development in mammals. J Dairy Sci 1986;69:3:927 — 943. 16. Romeis B. Mikroskopische Technik. Leibniz Verlag. Munchen 1948;159. 17. Webb R., Gauld I.K., Driancourt M.A. Morphological and functional characterization of large antral follicles in three breeds of sheep with different ovulation rates. J Reprod Fert 1989;87:243 — 255. Т.А. Смирнова, Л.Д. Галиева Всероссийский институт генетики и разведения сельскохозяйственных животных, Ст.-Петербург, г. Пушкин |