Влияние аномальной организации хроматина сперматозоидов
|
Стандартные клинические методы диагностики нарушения сперматогенеза связаны с анализом концентрации сперматозоидов, их подвижности и морфологии [1]. В последние годы появился новый способ оценки строгой морфологии сперматозоидов, позволяющий предсказать частоту оплодотворения в культуре, а также были предложены методы определения способности cперматозоидов к связыванию c блестящей оболочкой ооцитов [2, 3]. Эти методы характеризуют причины, препятствующие слиянию половых клеток. Если бы все причины мужского бесплодия сводились только к подобным дефектам, то они легко преодолевались бы оплодотворением в культуре (ЭКО). Применение ICSI должно было бы решить все проблемы. Несмотря на то, что ЭКО действительно облегчает слияние клеток, получить беременность иногда не удается даже после многократных попыток. Возможно, одной из причин могут являться нарушения в самой организации переносимого генетического материала, что может препятствовать последующим за слиянием половых клеток процессам развития.
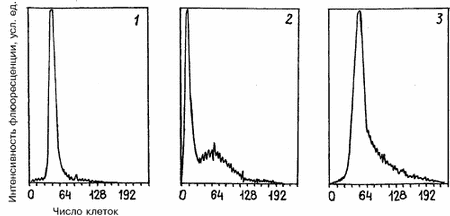
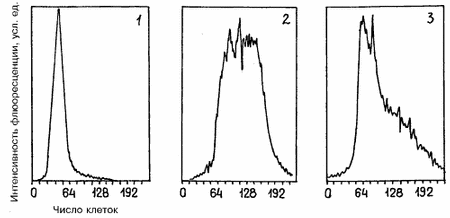
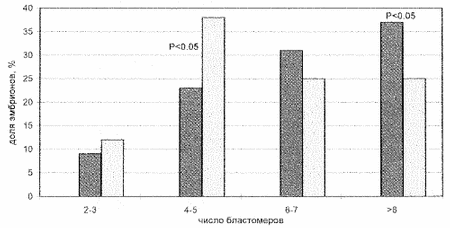
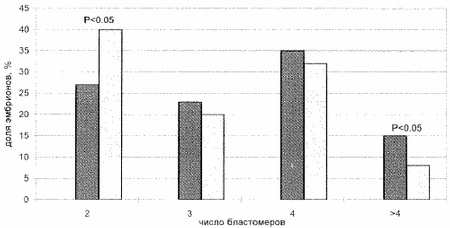
В литературе существуют указания на корреляцию между нарушениями в организации ядер спермиев и их способностью к оплодотворению [4–7]. В настоящее время на практике используется методика оценки организации хроматина ядер спермиев, основанная на полихромной окраске ядер акридиновым оранжевым [8, 9]. Однако этот метод можно расценивать как эмпирический, поскольку механизм действия красителя не ясен, а методика окрашивания мало стандартизирована. Нами разработан простой, легко интерпретируемый, количественный метод оценки интактности организации ядерного материала спермиев, пригодный для клинического использования. Основой метода явилось то, что ключевой момент плотной упаковки хроматина спермиев – поперечное сшивание протаминов дисульфидными связями – является завершающим этапом дифференцировки спермиев и важно для их функции. Для оценки степени компактизации хроматина ядер спермиев использовался эффект экранирования белками хроматина связывания с ДНК флюоресцентного красителя этидия бромида. Попытка экстрагировать из хроматина основные белки путем обработки полианионами (гепарином) без размыкания дисульфидных связей приводит к удалению той части белков, которая не была сшита поперечными ковалентными дисульфидными мостиками. В результате доступность ДНК для связывания этидия бромида возрастает. Таким образом, связывание этидия бромида с ДНК отдельных клеток, измеряемое методом проточной цитофлюорометрии, может служить мерой эффективности компактизации хроматина спермия в процессе дифференцировки. Данные о влиянии степени компактизации хроматина сперматозоидов на процессы оплодотворения и эмбрионального развития в культуре достаточно противоречивы. Большинство авторов считают, что тесты, оценивающие состояние хроматина мужских половых клеток, позволяют прогнозировать способность сперматозоидов к оплодотворению и могут иметь диагностическое значение [4]. Некоторые авторы не выявили взаимосвязи этих параметров [10]. В большинстве работ дается субъективная оценка состояния хроматина по степени окрашиваемости ядер анилиновым синим, акридиновым оранжевым или же по тесту на деконденсацию хроматина, что затрудняет интерпретацию полученных результатов. Использование флюорохрома хромомицина показало, что при наличии в эякуляте сперматозоидов с дефектами в организации хроматина повышается частота нарушения деконденсации их ядер в цитоплазме ооцитов после ICSI [5], а также уменьшается частота оплодотворения после инъекции сперматозоидов с помощью микроманипулятора под блестящую оболочку – SUZI [7]. Материал и методы Методом проточной цитофотометрии проанализировано 176 образцов спермы пациентов, проходящих лечение бесплодия в программе ЭКО в Центре репродукции ЭКО (Институт акушерства и гинекологии РАМН и Чикагский институт репродуктивной генетики). Для получения зрелых яйцеклеток применяли стимуляцию фолликулогенеза с помощью гонадотропных гормонов [12]. Для культивирования использовали среду Ham F-10 с альбумином человека и синтетическим заменителем сыворотки фирмы “Medi-Cult” (Дания). Выделение прогрессивно подвижной фракции сперматозоидов проводили в перколле. Для оплодотворения в среду к ооцитам вводили 100 000 сперматозоидов. Оплодотворение определяли через 18 ч после введения сперматозоидов по наличию двух пронуклеусов. Частоту оплодотворения рассчитывали как отношение числа зигот к числу ооцитов. Вычисляли долю эмбрионов с нормальной морфологией – без фрагментации бластомеров. Число бластомеров в эмбрионах определяли через 24 и 48 ч после образования пронуклеусов. Нормальными показателями спермограммы считали концентрацию сперматозоидов 20 млн и более в 1 мл, долю прогрессивно подвижной фракции более 40% и морфологически нормальных форм – более 40%. Согласно нашей методике, степень компактизации хроматина характеризуют гистограммы распределения клеток по способности связывать краситель (этидия бромид) до и после обработки гепарином. В норме почти все клетки окрашиваются одинаково и имеют низкую интенсивность флюоресценции, которая после обработки гепарином увеличивается примерно в 2 раза. Если у значительной части клеток (более 30) интенсивность флюоресценции повышена исходно либо после экстракции ковалентно несвязанных белков хроматина гепарином она возрастает в 2 раза и выше более чем у 50 клеток, то такие образцы спермы считали дефектными. Достоверность различий определяли по критерию c2 и t-критерию Фишера. Результаты Наиболее характерные проточно-цитофлюорометрические гистограммы приведены на рис. 1. Основываясь на выработанных критериях, мы проанализировали 176 образцов спермы пациентов программы ЭКО. Все пациенты были разделены на две группы – с нормальной (1-я) и аномальной (2-я) степенью компактизации хроматина сперматозоидов. Также были выделены подгруппы с нормальными показателями сперматогенеза и с патоспермией. Средний возраст женщин в группах не различался и составлял 31,3‰±4,1 года в 1-й и 31,9±4,8 года во 2-й группе. Полученные результаты приведены в таблице. Частота оплодотворения ооцитов у пациентов с нормальными показателями спермограммы не различалась независимо от состояния хроматина сперматозоидов. Однако у пациентов с измененными показателями спермограммы при аномальном характере хроматина частота оплодотворения снижалась по сравнению с пациентами, у которых этот параметр был в пределах нормы. Частота оплодотворения в культуре при патоспермии, но нормальном состоянии хроматина не отличалась от таковой при нормоспермии и составляла более 60%. Во всех подгруппах морфология эмбрионов не различалась по степени выраженности процесса фрагментации бластомеров. Для анализа влияния степени компактизации хроматина ядер сперматозоидов на динамику развития эмбрионов в культуре проанализировано число бластомеров в эмбрионах в различные сроки после начала культивирования у пациентов с нормальными показателями спермограммы. Полученные данные приведены на рис. 2. Число бластомеров в эмбрионах после 24 и 48 ч культивирования было достоверно выше у пациентов с нормальным уровнем компактизации хроматина в сперматозоидах. Таким образом, при аномалиях в организации хроматина замедляется процесс дробления эмбрионов в культуре. Рис. 1. Характеристика состояния хроматина ядер сперматозоидов человека, полученная методом проточн.
Рис. 2. Динамика 24(а)-48(б) часового развития эмбрионов in vitro.
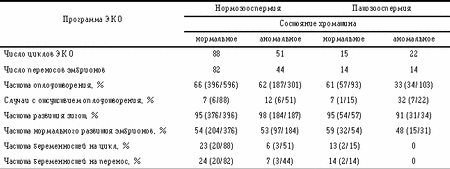
При нормальных показателях спермограммы частота наступления беременности также была достоверно выше у супружеских пар с нормальной компактизацией хроматина ядер сперматозоидов и составила в расчете на перенос эмбрионов 24% (во 2-й группе – 7%; см. таблицу). При патоспермии при нормальной компактизации хроматина ядер сперматозоидов частота наступления беременности в расчете на перенос эмбрионов составила 14%, а в группе с аномальным состоянием хроматина беременность получить не удалось. Таким образом, при аномалиях в структуре хроматина ядер сперматозоидов частота наступления беременности уменьшалась. Состояние хроматина ядер сперматозоидов и результаты лечения бесплодия в программе ЭКО
Обсуждение Связь нарушений организации генетического материала мужских половых клеток с бесплодием представляет собой как общебиологическую, так и важную медицинскую проблему. Общебиологическую – поскольку выбраковка эмбрионов с отклонениями в организации генетического материала в процессе ранних этапов развития могла бы играть роль фильтра, исключающего серьезные аномалии развития. Значение этого гипотетического механизма для понимания процесса онтогенеза и генетики популяций трудно переоценить. Медицинскую – потому что может выявлять случаи мужского бесплодия, обусловленные не только изменением показателей нормальной спермограммы, морфологии или неспособностью сперматозоидов связываться с блестящей оболочкой ооцитов, но и отклонениями в организации их генетического материала. Причины, ведущие к нарушениям в упаковке хроматина спермиев, сегодня не ясны. Вероятно, наиболее частой причиной этих нарушений являются не наследственные генетические изменения, а нарушения сперматогенеза в результате каких-либо патологических процессов или неблагоприятных воздействий окружающей среды. Эти факторы могут приводить либо к нарушениям созревания и увеличению числа незрелых форм, либо к нарушениям в упаковке хроматина у вполне зрелых спермиев. Не исключая значения первого из этих процессов, наши результаты свидетельствуют о доминировании второго механизма, поскольку незрелые формы спермиев не могут участвовать в оплодотворении. Благодаря разработанному количественному методу определения степени компактизации хроматина нам удалось исследовать вопрос о его влиянии на раннее развитие эмбрионов человека. Данные литературы о возможной взаимосвязи этих двух показателей достаточно противоречивы. Это существенно связано с применением разных методов выявления дефектов организации хроматина и высокой степенью субъективизма в анализе результатов. Некоторые авторы обнаружили снижение частоты оплодотворения в культуре при увеличении в эякуляте доли сперматозоидов с “незрелыми” ядрами [4]. Однако в других работах такой взаимосвязи обнаружить не удалось. В то же время частота оплодотворения при использовании метода SUZI была достоверно ниже в тех случаях, когда в эякуляте отмечена повышенная доля сперматозоидов с изменениями в структуре хроматина [7]. В программе ICSI в таких случаях отмечено повышение доли неконденсированных ядер сперматозоидов в цитоплазме неоплодотворенных ооцитов [5]. Вопрос о влиянии состояния хроматина сперматозоидов на эмбриональное развитие изучен крайне недостаточно. Возможность получения беременности при увеличении в эякуляте сперматозоидов с аномальной структурой хроматина доказана. Однако сравнительных количественных данных нам найти не удалось [7]. В программе ICSI применяется инъекция незрелых гамет, при этом частота наступления беременности ниже в тех случаях, когда эти клетки выделяют из более дистальных участков эпидидимиса [5]. В работе M. Ibrahim и соавт. [16] обнаружено, что у супружеских пар, у которых отмечена повышенная гетерогенность хроматина сперматозоидов, часто наблюдается привычное прерывание беременности на ранних сроках. При этом доля сперматозоидов с аномалиями в структуре хроматина превышает 39%, а этот показатель у фертильных доноров не выше 9%. При использовании в программе ICSI тестикулярных сперматозоидов способность эмбрионов к имплантации была существенно ниже, чем при использовании эпидидимальных сперматозоидов [17]. В серии работ D. Evenson и соавт. [8, 13] доказывается взаимосвязь повышения доли сперматозоидов с нарушениями организации хроматина и мужского бесплодия. Аналогичные результаты получены и для сельскохозяйственных животных (быков). В одной из последних работ этих авторов показано наличие строгой корреляции между плодовитостью быков и структурой хроматина их сперматозоидов [6]. Таким образом, согласно нашим данным, аномалии в организации хроматина ядер сперматозоидов влияют на раннее развитие эмбрионов в программе ЭКО и частоту наступления беременности. Известно, что экспрессия мужского генома происходит у эмбрионов человека на стадии 4–8 бластомеров. Возможно, что аномалии в механизмах, контролирующих компактизацию хроматина, сказываются уже на ранних стадиях развития эмбрионов, что проявляется в замедлении темпов дробления в культуре. На основании полученных результатов можно сделать заключение о существовании механизма прерывания ранних стадий развития эмбрионов в случаях нарушения организации генетического материала мужских половых клеток – аномальной компактизации хроматина. Можно также предложить простой и эффективный метод диагностики мужского бесплодия. Литература 1. Руководство ВОЗ по лабораторному исследованию спермы человека и взаимодействия спермы с цервикальной слизью. Тбилиси 1987; 21. 2. Воробьева О.А., Скрипкина О.А., Корсак В.С. Методы оценки морфологии сперматозоидов и их прогностическое значение в программе ЭКО. Пробл репрод 1995; 3: 71–76. 3. Воробьева О.А., Леонтьева О.А., Корсак В.С. Влияние морфологии сперматозоидов на частоту оплодотворения и нарушения развития эмбрионов в программе ЭКО. Цитология. 1996; 38: 12: 1248–1254. 4. Liu Y., Baker H.W.G. Sperm nuclear chromatin normality: relationship with sperm morphology, sperm – zona pellucida binding, and fertilization rates in vitro. Fert Steril 1992; 58: 6: 1178–1184. 5. Sakkas D., Urner E., Bianchi P.G., Bizzaro D. et al. Sperm chromatin anomalies can influence decondensation after intracytoplasmic sperm injection. Hum Reprod 1996; 4: 837–843. 6. Sailer B.L., Jost L.K., Evenson D.P. Bull sperm head morphometry related to abnormal chromatin structure and fertility. Cytometry 1996; 24: 167–173. 7. Bianchi P.G., Manicardi G.C., Urner F., Campana A., Sakkas D. 7. Bianchi P.G., Manicardi G.C., Urner F., Campana A., Sakkas D. Chromatin packaging and morphology in ejaculated human spermatozoa: evidence of hidden anomalies in normal spermatozoa. Mol Hum Reprod 1996; 2: 3: 139–144. 8. Evenson D.P., Darzynkewicz Z., Melamed M.R. Relation of mammalian sperm chromatin heterogeneity to fertility. Science. 1980; 240: 1131–1133. 9. Liu D.Y., Baker H.W.G. Tests of human sperm function and fertilization. Fert Steril 1992; 58: 3: 465–485. 10. Claassens О.E., Menkveld R., Franken D.R. et al. The acridine orange test: determing the relationship between sperm morphology and fertilization in vitro. Hum Reprod 1992; 7: 242–247. 11. Jeulin C.D., Feneux C., Serres P., Jouannet P. et al. Sperm factors related to failure of human in vitro fertilization. 1986; 76: 735–744. 12. Корсак В.С., Исакова Э.В., Воробьева О.А., Каменецкий Б.А., Кирсанов А.А. Применение золадекса (гозерелина) в схеме индукции суперовуляции в программе ЭКО. Пробл репрод 1996; 2: 3: 23–17. 13. Evenson D.P., Melamed M.R. Rapid analysis of normal and abnormal cell types in human semen and testis biopsies by flow cytometry. J Histochem Cytochem 1983; 31: 248–253. 14. Liu D.V., Baker H.W.G. Test of human sperm function and fertilization in vitro. Fertil Steril 1992; 58: 58: 3: 455–473. 15. Schlegel P.N., Alikani M., Berkeley A.S. Epididymal micro- puncture with in vitro fertilization and oocyte micromani- pulation for the treatment of unreconstructable obstructive azospermia. Fertil Steril 1994; 61: 895–901. 16. Ibrahim M.E., Moussa M.A., Pedersen H. Sperm chromatin hete- rogeneity as an infertility factor. Arch Androl 1988; 21: 129–133. 17. Vanderzwalmen P. et al. Частота оплодотворения и беременности после интрацитоплазматической инъекции сперматозоида (ICSI) при использовании эякулированных, эпидидимальных и тестикулярных сперматозоидов. Пробл репрод 1995; 2: 52–60. О.А. Воробьева, М.В. Филатов, О.А. Леонтьева, Е.В. Семенова Институт акушерства и гинекологии им. Д.О. Отта, Центр ЭКО, Институт ядерной физики им. А.К. Константинова РАН, С.-Петербург |