Развитие эмбриона человека и некоторые морально-этические проблемы методов вспомогательной репродукции
|
В 1978 г. в Англии родилась Элиза Браун — первый ребенок, зачатый в результате экстракорпорального оплодотворения (ЭКО) и в виде эмбриона перенесенный (ПЭ) в матку матери на ранних этапах дробления [77]. К настоящему времени с помощью методов вспомогательных репродуктивных технологий (ВРТ), обеспечивающих оплодотворение яйцеклетки вне организма в случаях невозможности такового естественным путем, рождены многие тысячи детей. ВРТ непрерывно совершенствуются и все большее число людей с их помощью решают проблему деторождения. Разработаны методы криоконсервации эмбрионов и половых клеток, срок хранения которых оговорен от 5 до 10 лет [21,80, 81].
Кроме лечения многих форм мужского и женского бесплодия, ВРТ используются и для решения проблем фундаментальной биологии и медицины. Используя не затребованные для ипмлантации эмбрионы, изучают механизмы оплодотворения и развития эмбриона, генетическую регуляцию эмбриогенеза, возможности преимплантационной диагностики наследственных заболеваний и другие проблемы. В Англии существует положение, по которому использование так называемых «лишних» эмбрионов допускается только при разрешении матери или обоих родителей [ 21]. Cреди клиницистов, исследователей и в кругах общественности (особенно среди представителей разных конфессий) отношение к использованию ВРТ для терапевтических и исследовательских целей неоднозначно. Даже в странах, в которых нормативно и законодательно регулируется и контролируется деятельность специалистов и учреждений по ВРТ, использование последних вызывает крайне противоречивые оценки [14, 21]. В странах, где отсутствуют нормативные акты по применению новых ВРТ (например, в СНГ), не только сами исследователи, но и лица, для которых они используются, не могут быть гарантированы от конфликтных ситуаций. Например, при выполнении селекции эмбрионов при многоплодной беременности (более 3 эмбрионов одновременно трансплантировать не рекомендовано) [21], выборе пола плода без медицинских на то показаний и пр. О недостаточной осведомленности отечественных специалистов — медиков и биологов относительно морально-этических аспектов ВРТ и возможностей их корректного решения свидетельствуют и данные проведенного нами анкетирования [12]. Об этом же свидетельствуют прошедшие в конце 1997 г.— начале 1998 г. обсуждения (в том числе в некоторых комитетах Госдумы РФ) и публикации в СМИ, посвященные проблемам биомедицинской этики, клонирования животных и человека [6, 82]. Cторонники так называемой абсолютистской позиции, основываясь на моральных и религиозных принципах, требуют запрета любых манипуляций с эмбрионами на любых стадиях развития, поскольку считают, что эмбрион — это существо, имеющее душу с момента оплодотворения. Высказывается мнение о том, что дальнейшее развитие ВРТ несет опасность генофонду, здоровью человечества, поскольку отдаленные последствия ВРТ еще не выявлены. Выдвигаются требования установления жестких критериев, ограничивающих применение ВРТ. Приверженцы противоположной точки зрения призывают к широкому внедрению ВРТ в качестве альтернативного естественному способу размножения людей. При более разумной, умеренной (градуалистической) позиции, которую занимают многие ведущие специалисты в области медицины — эмбриологи, генетики, репродуктологи, философы, социологи и законодатели, в правовой защите нуждается развивающийся эмбрион, когда приобретает черты и свойства, характерные для личности [45]. Согласно этой позиции, ВРТ в терапевтических и исследовательских целях допускаются по строгой регламентации при разработке законодательных актов, широком контроле и информированности общественности и одобрении специальными контролирующими институтами. Примером такого регулирования может служить специальный правительственный комитет, созданный в Англии в 1982 г., а затем и институт (в 1990 г.), целью которого является контроль за эмбрионами человека, их использованием с терапевтическими и исследовательскими целями и разработка рекомендаций правительству для специального законодательства [21, 80, 81]. Эти мероприятия обеспечивают в Англии защиту эмбриона, позволяют проводить ежегодный контроль учреждений, выполняющих ВРТ. Эмбрионы для целей ВРТ используются до 14 дней развития и в случае проведения исследований после их завершения обязательно разрушаются. Наличие в Англии соответствующего законодательства исключает дискриминацию бесплодных пар и рожденного с помощью ВРТ ребенка [21, 33, 80, 81]. Ключевая морально-этическая проблема ВРТ—статус эмбриона, с какого момента его следует рассматривать как личность, имеющую право на жизнь и ее защиту в законодательном порядке. К другим обсуждаемым в научной печати проблемам относятся правомерность манипуляций с гаметами и эмбрионами с терапевтическими и исследовательскими целями, замораживание половых клеток и эмбрионов и их использование реципиентами, анонимность доноров гамет, эмбрионов суррогатных матерей, их права и обязанности; выбор пола плода при риске носительства связанных с полом заболеваний и т.п. [13, 14, 24, 33, 38—40, 43, 47, 51, 57, 58, 69, 73, 76]. В настоящем сообщении мы рассмотрим ключевую проблему ВРТ — статус эмбриона человека. С какого момента развития эмбрион человека должен рассматриваться как личность? По каким критериям необходимо решать проблему определения личности, статуса эмбриона и/или гамет? Гаметогенез и естественная селекция половых клеток. Оогенез Первичные половые клетки (ППК, или гоноциты) имеют внегонадное происхождение. Они обособляются на задней стенке первичной кишки от прочих клеток формирующегося эмбриона и мигрируют в область зачатка половых желез, формирующихся на вентральной стороне мезонефроса (первичной почки). По морфологическим критериям (более крупным, чем соседние соматические клетки, размерам и округлой форме) и наличию гликогена и щелочной фосфатазы они идентифицируются уже у зародышей VII—IX стадии развития (по Стриттеру) — 15—20-дневных эмбрионов человека [17]. Дифференцировка гонад по полу, т.е. появление морфологических различий в их структуре, позволяющих идентифицировать яичники от яичек (женский от мужского гонадного пола, соответственно), отмечена уже у 6-недельных эмбрионов [10, 11, 18]. У эмбрионов-плодов женского пола после заселения гонад гоноцитами последние делятся митозом, трансформируются в оогонии, которые также делятся митотически много раз и создают пул половых клеток. Число женских половых клеток в яичнике в течение всей дальнейшей жизни женского организма более не пополняется, а лишь расходуется: посредством ежемесячной овуляции единичных ооцитов в половозрелый период и столь же регулярной атрезии 10—15 других, менее созревших к моменту овуляторного пика ЛГ, а также ооцитов из фолликулов более ранних стадий развития — от примордиальных до мелких полостных, дегенерирующих по разным причинам [10—12,22, 52]. Так, у 4-месячного плода человека количество половых клеток в яичнике достигает максимума — 2—3 млн. [22]. По мере формирования этого пула гоноциты превращаются в оогонии, затем — в ооциты I, претерпевающие важные генетические события гаметогенеза (схему оогенеза человека см. Проблемы Репродукции № 2, 1996, стр.64.) — рекомбинацию наследственных структур в профазе мейоза I. Затем, по мере завершения этих этапов ооциты окружаются фолликулярными клетками: только вокруг ооцитов в диплотене развивается фолликулообразование [10, 11, 52] и создается новый гематофолликулярный барьер — защита ооцитов от повреждающих воздействий. Таким образом, плод женского пола рождается со сформированными для гамет барьером и пулом половых клеток. Далее, при наступлении половой зрелости в рост под влиянием гормонов вступает 10—15 ооцитов (в фолликулах), и такое пополнение растущих фолликулов происходит непрерывно, до полного их расходования и наступления менопаузы. Дегенерирующие (атрезирующиеся) фолликулы выполняют эндокринную функцию. В целом за весь репродуктивный период жизни женщины может в среднем овулировать 400—450 ооцитов, а реально дать жизнь новому индивидууму — 15—20 ооцитов, остальные погибают на всех этапах своего развития [11, 12, 53]. Конкретные причины их гибели разнообразны, практически не исследованы. Установлено лишь, что до 1/3 ооцитов в пахитене имеют нарушение определенной структуры мейотических хромосом — синаптонемного комплекса (СК) [21], что может явиться причиной их гибели. На уровне светового микроскопа нами установлено, что около 1/6 — 1/4 ооцитов после пахитены вступают в дегенерацию. Т.е. дегенерация, гибель половых клеток происходит на всех этапах их развития, но особенно интенсивно начинается — после завершения 1-го этапа генетической рекомбинации — после пахитены профазы мейоза I [12, 52,53]. Вышесказанное свидетельствует о том, что скорее всего дегенерируют именно те гаметы, в которых имелись генные и хромосомные нарушения, произошедшие за предшествующий период развития или переданные от родителей. Нельзя исключить вероятность того, что развивающиеся дегенеративные изменения приводят к возникновению генных и хромосомных мутаций в гаметах, что, в свою очередь, является причиной гибели большей части таких гамет. Достигают созревания лишь наиболее жизнеспособные ооциты. Основная биологическая роль женских половых клеток — не только снабжение следующего поколения генетической программой жизни (через гаплоидный набор хромосом), но и обеспечение (после оплодотворения) эмбриона питанием и энергией на первых этапах его развития, до его имплантации в матку. Подготовка к этой второй роли начинается задолго до оплодотворения, еще во внутриутробный период жизни женского организма и завершается незадолго до овуляции в половозрелом периоде. Схематично она осуществляется через синтез большого количества РНК и позднее с ее помощью белка — идущего не столько на построение формирующейся яйцеклетки, сколько на питание и поддержание жизнеспособности доимплантационного эмбриона (см. рис.1). Сперматогенез (схему сперматогенеза у млекопитающих и человека см. Проблемы Репродукции №3, 1995, стр. 34.) У эмбрионов человека мужского пола мигрирующие в гонады гоноциты также делятся несколько раз, преобразуясь в просперматогонии, создают некоторое число (определенный, но не окончательный пул) половых клеток и затем сперматогенез останавливается на этом начальном этапе и возобновляется (продолжается) уже при наступлении полового созревания [1, 19]. К указанному возрасту в яичках начинает формироваться гематотестикулярный барьер, обеспечивающий защиту половых клеток от повреждающих воздействий, защиту яичек от пораженных гамет и способствующий элиминации поврежденных гамет [16,29, 55]. За одну эякуляцию (в среднем 2—4 мл эякулята) выходит в среднем 40—400 млн. сперматозоидов, один из них участвует в оплодотворении, остальные — погибают. За всю репродуктивную жизнь человека (в среднем 40—50 лет) в яичках формируется в среднем 80—180 в 10-й степени сперматозоидов (т.е. около 800—1800 триллионов), и лишь единичные из них участвуют в оплодотворении. Основная функция зрелых мужских половых клеток — доставить гаплоидный набор хромосом мужской гаметы (с уникальной генетической программой развития) через продвижение сперматозоида к яйцеклетке, контакт с нею и проникновение сперматозоида через оболочки яйцеклетки в ее цитоплазму. И весь длительный и многоэтапный сперматогенез направлен на становление и осуществление такой функции. Доля гамет, не развившихся до зрелых сперматозоидов, не известна. Как и в оогенезе, в сперматогенезе идет активная селекция клеток на всех этапах их развития, о конкретных причинах гибели гамет и доле каждой из причин в общем числе дегенерирующих гамет не известно. Определено лишь, что в яичках эмбрионов и плодов до 20—25% просперматогониев имеют аномалии митотического деления (являющиеся одной из причин возникновения хромосомных мутаций, аберраций -ХА- в гаметах) [19]. Начинает обсуждаться принципиальный и важный для теоретической биологии (и для медицинской репродуктологии, гаметологии) вопрос — каково число митотических делений в ППК, у оогониев и сперматогониев, особенно в свете последних открытий о роли теломеразы в регуляции клеточных делений. Среди сперматоцитов I в пахитене у 20% выявлены нарушения СК [78]. Эти гаметы являются реальными кандидатами в дальнейшую дегенерацию и гибель. Установлено, что 10% зрелых сперматозоидов здоровых мужчин детородного возраста имеют различные числовые и структурные ХА [56]. Очевидно, что по мере прохождения гаметами (и женскими и мужскими) этапов дифференцировки половые клетки с ХА претерпевают дегенерацию и селекцию. Таким образом, на более поздних стадиях гаметогенеза меньшее число гамет содержит нарушения хромосом. Вероятно, что подобная же селекция (уменьшение числа гамет с определенными типами нарушений по мере продвижения их по этапам дифференцировки) происходит с гаметами, несущими генные мутации, имеющими нарушение физиологии нехромосомных структур клетки [2, 3]. Т.е. высока случайность участия той или иной половой зрелой клетки в оплодотворении, приводящем (далеко не всегда) к развитию и рождению нового индивидуума. Специалист по медицинской этике, профессор G. Hermeren [45] полагает, что вероятность участия сперматозоида в оплодотворении 1 на 2 млн., а шанс развития оплодотворенной яйцеклетки до рождения ребенка — примерно 1 на 80 [64]. Мы полагаем, что первые цифры занижены, вероятность участия сперматозоида в оплодотворении — 1 на 40—400 млн. Естественная селекция, упомянутая выше для гамет, продолжается и далее — на уровне оплодотворения, доимплантационного развития, разных сроков внутриутробного развития. Установлено, что более 50% всех зачатий элиминируется до установления факта беременности [46]; 50—60% спонтанных абортусов имеют ХА [25,26,35]. Среди живорожденных и в популяции взрослого населения в среднем 0,5—0,7% индивидуумов имеют ХА [8, 50]. Т.е. по мере продвижения развития в онтогенезе, как и в гаметогенезе, доля индивидуумов с ХА снижается. Общеизвестны факты недоношенности детей (рождение ребенка до 34-й недели беременности, массой до 2500 г) —5 —10% от числа живорожденных. Отмечено, что около 60% летальности новорожденных приходится именно на долю недоношенных детей [23,27]. Оплодотворение и внутриутробное развитие человека Оплодотворение — процесс взаимодействия мужской и женской зрелых гаплоидных половых клеток, вследствие которого развивается новый организм с диплоидным набором хромосом. Хромосомы содержат уникальную генетическую программу развития, полученную через гаплоидные наборы хромосом яйцеклетки и сперматозоида. После оплодотворения яйцеклетка путем многих митотических делений развивается в многоклеточный организм. Представим основные положения внутриутробного развития человека из фундаментальных руководств [5,18,23,30,39,60, 67,68], дополненные сообщениями последних 15 лет [4,17,28,32,70,71,79] и собственными наблюдениями.
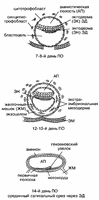
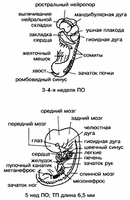
Первые стадии дробления зиготы происходят в маточной трубе, через 1—2,5 сут. после овуляции ооцита (рис.1). Описана стадия слияния пронуклеусов оплодотворенной яйцеклетки — примерно 20-часовой преэмбрион человека [4]. Случайные находки исследователей двухклеточного эмбриона человека (36 ч после оплодотворения) и четырехклеточного позволили описать наличие плотных десмосомоподобных соединений между бластомерами и специфическое расположение цитоплазматических органелл. Подчеркивается формирование пузырьковидных структур на ядерных мембранах двухклеточного эмбриона и на наружной мембране бластомеров и ядерной мембране четырехклеточного эмбриона [70,71], а также тесный контакт ядерной мембраны и цитоплазматического ретикулума. При изучении ультраструктуры морулы на стадии 16 клеток (через 3 дня после овуляции) отмечено различие между бластомерами по форме, но не по размерам, наличие плотных десмосомоподобных контактов между бластомерами, активность базолатеральной клеточной мембраны, состояние митохондрий, паракристаллических структур, функционально активных ядрышек [70]. Информация об экспрессии генома на ранних стадиях развития не только человека, но и млекопитающих крайне ограничена, несмотря на высокую значимость такой информации для теории и практики (сроки начала функционирования генома эмбриона, механизмы процессинга мРНК на первых этапах дробления и др.), а также для решения ряда вопросов биомедицинской этики. Разработка методов ЭКО облегчила возможности изучения этой проблемы [32, 34]. Полагают, что собственно геном яйцеклетки функционирует при первых двух дроблениях зиготы, затем в регуляцию развития включается геном сперматозоида и в восьмиклеточном эмбрионе начинается функционирование генома эмбриона. Эти данные носят предположительный характер и проблема ждет своих исследователей [28]. На 3-й день после овуляции (ПО) эмбрион дробится до стадии морулы — компактной многоклеточной структуры шарообразной формы (см. рис.3). На 4-й день ПО формируется бластула (бластоциста) — многоклеточное шаровидное образование с полостью внутри (бластоцель) (см. рис. 3). На одном из ее полюсов, изнутри определяют скопление клеток — внутреннюю клеточную массу (ВКМ), из которой развиваются зародыш, амнион, желточный мешок и аллантоис. Из наружного одноклеточного слоя бластоцисты формируется трофобласт (хорион) и в дальнейшем — плодовая часть плаценты. К 6-му дню ПО бластоциста освобождается от прозрачной оболочки (как бы вылупляется из нее), лишается определенного защитного барьера, который был бы помехой при имплантации. Считают, что имплантация начинается с 6-го дня ПО, когда бластоциста спускается в полость матки и начинает прикрепляться к эндометрию. На 7—8-й день формируется полость амниона, различают эктодерму и энтодерму — такой двуслойный зародыш называется стадией эмбрионального (зародышевого) диска, он глубже имплантируется в эндометрий, усложняются его внезародышевые оболочки (рис. 2), начинает формироваться плацента. До 14-го дня ПО ведущие эмбриологи мира рассматривают эмбрион человека как проэмбрион, считая, что до этого срока он сформирован клеточными слоями, представляющими собой зародышевые оболочки, материал, не участвующий в построении в дальнейшем собственно эмбриона [36,37,57, 58]. На 14—15-й день определена ось зародышевого диска, формируется первичная полоска гензеновский узелок, закладка хорды (см. рис. 4), т.е. это срок начала формирования элементов нервной системы эмбриона человека. На 16-й день определяется первичный желточный мешок и первичная мезодерма, на 18-й — дефинитивный желточный мешок, прехордальная пластинка и хорда. На головном конце зародышевого диска выражены нервные валики. У 1/4 из всех изученных эмбрионов этого срока развития на дорcальной поверхности описаны клетки нервной пластинки [23, 30, 39, 60, 67, 68]. На 19—20-й день определяются нервные валики, на 22-й день начинает формироваться нервная трубка. К этому сроку длина эмбриона достигает 3 мм, происходит образование сомитов (путем сегментации осевой мезодермы). Во внутризародышевой мезодерме формируется полость перикарда и внутризародышевый целом; развиваются зачатки сердца, легких, щитовидной железы, пупочных сосудов. В открытой нервной трубке уже намечаются передний, средний и задний мозговые пузыри (рис. 3). Формируется слуховая плакода и зрительная борозда, выявлены мандибулярная и гиоидная дуги; идет отделение хорды от подлежащей энтодермы; различимы передняя, средняя и задняя кишка. Определяется эндокард и миокард, формирующееся сердце сокращается. Образуется целом, отдельные элементы крови (из мезодермы желточного мешка), устанавливается замкнутое кровообращение через желточный мешок и ножку зародыша [5, 18, 30, 39, 60, 67, 68].
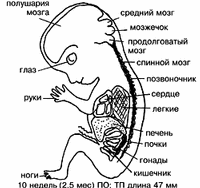
В период между 21-м и 32-м днем ПО продолжается и затем завершается сегментация (сомитогенез), выявляются 25 пар сомитов. Устанавливается односторонний ток крови через сердце. Определяются зачатки рук и ног, обонятельные плакоды, продолжается органогенез глаз и уха; в замкнутой нервной трубке четко различаются отделы мозга и обозначены полушария головного мозга и мозжечка. Формируются нервы от двигательных областей спинного мозга и спинальных ганглиев. Сформирована первичная почка (мезонефрос); определяются зачатки мочеточника (в виде выростов мезонефральных протоков), открывающихся в клоаку (мочеполовой синус), и половые валики (складки) — зачатки половых желез, а также печень, желчный пузырь, поджелудочная железа, различные отделы кишечного тракта. Почти завершается подразделение сердца на камеры, сердце функционирует (см. рис.5) [23, 67, 68]. Длина эмбриона 40—42 дней ПО достигает 22 мм. Более выражены структуры головного отдела; сформированы пять первичных отделов мозга. В области глаза начинается дифференцировка нервного слоя на различные ряды клеток; прогрессируют в развитии структуры внутреннего уха. Различимы зачатки пальцев конечностей и локтевые сгибы, хвост, который в дальнейшем подвергается инволюции, верхняя и нижняя челюсти, сформированные ноздри; развивается наружное ухо. Происходит окостенение длинных трубчатых костей, осевого скелета и черепа. Формируются тимус, паращитовидные железы и ультимобранхиальные тельца.Сформировался единый клеточный зачаток языка, развиваются его мышцы. Происходит гистогенез органов пищеварительного тракта. Во вторичной почке (метанефросе) различают клубочки и канальцы [23, 67,68]. Морфология половых желез четко дифференцирована по полу [10,11,18]. Установлено начало двигательного поведения эмбриона человека [74]. Период до конца 8-й недели эмбриогенеза человека (длина эмбриона достигает 40 мм, масса — 0,5 г) характеризуется интенсивным ростом и дальнейшей дифференцировкой систем органов. В этот период вырисовываются черты лица, что придает эмбриону большее сходство с человеческим обликом; обособляется шея, формируются наружное ухо и наружные отделы носа, сформированы веки и все отделы конечностей, пальцы, исчезает хвост. Интенсивно развиваются большие полушария, в них различимы кора и базальные ганглии. Первичная почка (мезонефрос) подвергается инволюции, происходит формирование надпочечника. Наружные половые органы дифференцированы по полу. Конец 8-й недели внутриутробного развития знаменует окончание эмбрионального и начало плодного периода у человека. Дифференцированы основные структуры и системы органов [5, 23, 39, 67, 68]. Начинающийся с 9-й недели внутриутробного развития человека плодный период, завершающийся рождением плода, характеризуется его интенсивным ростом, дальнейшей дифференцировкой органов и систем (рис.4) и становлением их дифференцированных функций. На 10-й неделе наблюдается рефлекторное движение губ (развивается рефлекс сосания). На 12-й неделе внутриутробного развития плод достигает 87 мм в длину и весит около 45 г, приобретает все больше человеческих черт: по сформированным частям лица и головы. Рефлекторное движение пальцев конечностей в ответ на прикосновение свидетельствует о развитии соответствующих центральных нейронных связей. Развиваются также нервные механизмы некоторых спинальных рефлексов плода. Отмечены дыхательные движения последнего. У 16-недельного плода человека сформировано большинство костей тела, прогрессирует их окостенение, полностью функционирует вторичная почка. Пищеварительный тракт начинает функционировать в период между 16-й и 20-й неделей развития. На 20-й неделе начинается гемопоэз в костном мозге. Дальнейшее развитие плода человека — 20—38-я неделя беременности — характеризуются продолжающейся гистологической, анатомической и функциональной дифференцировкой органов и систем плода: его рост замедляется, образуется волосяной покров и развивается функционирование сальных желез кожи. У плода мужского пола на 7-м месяце начинается пассивное опускание яичек в мошонку вследствие разности скорости развития определенных соседних с ними анатомических структур. Нарушение этого процесса приводит к одно- или двустороннему крипторхизму. Функционируют органы чувств: выявлена реакция на свет, звук, вкусовые и обонятельные раздражители [23,68]. Одним из ключевых в определении возраста эмбриона человека как личности является вопрос о том, когда плод человека приобретает способность чувствовать? Первые движения плода зафиксированы на 6-й неделе развития [74], в это же время плод реагирует на прикосновения, в спинном мозге выявляются синапсы. В нервных волокнах спинного мозга у плода 10-й недели развития определены первые нейромедиаторы и зарегистрирована активность ствола головного мозга. На основании данных электрофизиологических и иммунологистохимических исследований центральной и периферической нервной системы [79] высказано мнение о том, что плод человека начинает чувствовать в возрасте 18—25 нед, но до 30-й недели развития отсутствуют доказательства способности плода перерабатывать полученные ощущения. Автор рассматривает 30-ю неделю развития нижней границей между плодом и человеческим существом [79]. Поскольку полноценное функционирование мозга (а по каким критериям это определяется, где граница перехода в неполноценую функцию?) наступает у человека после первых 2 лет жизни (определение психиатров), некоторые исследователи считают, что разговор об эмбрионе как личности — не состоятелен. Другие предлагают как личность рассматривать плод после 7 мес, когда он приобретает способность жить самостоятельно (вернее — изолированно) вне тела матери. C. Grobstein [43] в качестве критерия определения возраста, с которого эмбрион можно рассматривать как личность, предлагает учитывать его способность реагировать на раздражение или причиняемую ему боль, что проявляется у 6— 8-недельного эмбриона. Horan (1977) считает неправомочным принимать за такой критерий реакцию плода на раздражение, так как считает, что бессознательное состояние и нечувствительность к боли не могут служить основанием для отказа в защите прав личности. Проблема определения возраста, с которого эмбрион человека можно рассматривать как личность, обладающую правами (в первую очередь — на жизнь) и защищаемую законодательством, возникает в ходе обсуждения вопроса о возможности осуществления различных манипуляций с эмбрионами. Под понятием «манипуляции с эмбрионом человека» подразумевают: культивирование их in vitro для терапевтических (лечение бесплодия) и исследовательских (улучшение условий культивирования, разработка новых методов диагностики и пр., изучение закономерностей оплодотворения и развития) целей, отработка условий и проведение глубокого замораживания гамет и эмбрионов и хранение их в таком состоянии с последующим их использованием для выполнения практической программы ЭКО или в научных целях. Правомочность выполнения таких манипуляций и степень допустимого воздействия на эмбрионы человека широко обсуждаются в специальной и популярной литературе и правительствами ряда стран [13—15, 20, 33, 35—38, 45, 47, 51, 53, 57, 58, 69, 76, 80, 81]. В силу недостаточной изученности всех аспектов (медицинских, биологических, социальных, правовых, морально-этических, философских) данной проблемы оказывается невозможным прогнозирование отдаленных последствий для здоровья отдельного индивидуума, потомства, популяции, социума и т.д. любых манипуляций с эмбрионами и ВРТ в целом. Культивирование эмбрионов человека in vitro для лечебных целей является необходимым условием осуществления ЭКО. Проведение исследований имеет целью, во-первых, совершенствование техники ЭКО и в целом репродуктивной технологии как отрасли медицины; во-вторых, установление полноценности и отсутствия патологии эмбриона до момента переноса его в матку, т.е. профилактику рождения ребенка с генетической патологией. Перспективны методы преимплантационной диагностики (цитогенетической, биохимической, молекулярно-генетической) яйцеклеток (по полярным тельцам) и ранних доимплантационных (т.е. до бластоцисты) эмбрионов по бластомерам [44, 73]. Эти исследования возможны лишь на эмбрионах самых первых стадий развития, в условиях ЭКО. Обсуждается проблема относительно судьбы «лишних» гамет и, что важнее, эмбрионов, т.е. не использованных для данной супружеской пары яйцеклеток и доимплантационных эмбрионов. В свете дискуссий о статусе эмбриона человека встает вопрос о том, что является более гуманным: подвергать их разрушению (как невостребованных) или проводить с ними исследования относительно общих закономерностей развития человека (эмбрионы недоступны при естественном оплодотворении для таких целей). При всестороннем обсуждении проблемы определения статуса эмбриона человека прежде всего встает вопрос о том, с какого момента эмбрион человека становится личностью? Жизнь человека начинается с момента оплодотворения. А душа? Душа — это Божий дар, и она вселяется в эмбрион также с момента оплодотворения, согласно христианской вере [40]. По Корану, вселение души, которая превращает живое существо в личность, происходит на 40-й день (или позднее...)[24]. Этичны ли вопросы, задаваемые многими: Ранний эмбрион — это начало жизни или начало жизни человека, личности? Ранний эмбрион — это масса недифференцированных клеток или душа? К понятию душа могут ли быть приложимы биологические критерии или это понятие морали, этики? Если жизнь священна, то моральная дилемма — определение статуса эмбриона человека — безнадежна. Известно, что на двух и четырехклеточной стадии бластомеры плюрипотентны (каждый бластомер способен развиться самостоятельно в эмбрион) и тотипотентны (каждый из бластомеров имеет возможность стать либо эмбрионом, либо — внезародышевой тканью). Известно, что монозиготные близнецы могут развиться из одной раздробившейся на 2 бластомера, оплодотворенной яйцеклетки, каждый бластомер от которой вступает на самостоятельное развитие в эмбрион [40]. Зарождение эмбриона — это 1 случай из множества случайных или неосуществленных возможностей (вследствие естественной селекции на уровне гамет, зигот, эмбрионов и т.д., рассмотренной выше) или дар Бога (догмат предопределения)? Этично ли обсуждать право эмбриона человека на жизнь и не говорить об охране права животного на жизнь? При обсуждении медико-биологических, морально-этических аспектов определения предельного возраста эмбриона, допустимого для использования в эксперименте, ведущие эмбриологи мира называют, как правило, период от момента оплодотворения (стадия зиготы) до 14-го дня развития (до начала формирования первичной полоски и появления элементов нервной системы) [36, 37, 57, 58] или срок до 30-го дня развития ( начала дифференцировки структур головного мозга). Отмечают, что эмбрион человека в системе in vitro не является законоправным субъектом и не имеет защиты. Эмбрион является общественным объектом, принадлежащим поставщикам гамет, и судьбу эмбриона решают они (или их наследники), хотя нельзя говорить об обычной, в общепринятом понимании, собственности. L. Honnefelder [47] полагает, что начало жизни, как и ее конец, не может рассматриваться как точка (момент) во времени, но как процесс. Подчеркивается необходимость различать генетическую уникальность эмбриона (со стадии зиготы) и онтогенетическую индивидуальность — при появлении первичной полоски [45]. Большая часть среди участвующих в обсуждении этой проблемы специалистов — медики, биологи, философы, социологи, правоведы, учитывая невозможность в настоящее время решить вопрос о статусе эмбриона человека и невозможность (нецелесообразность?) остановить использование ВРТ и некоторых аспектов биотехнологии (клонирование животных и пр., но не человека), придерживаются умеренной позиции. Согласно последней, в основе начала жизни лежит природа последовательных биологических процессов, и защита эмбриона человека соотносительна степени его развития [45]. Основные тезисы этой позиции следующие: 1) cперматозоид и яйцеклетка — живые организмы высокой сложности, и оплодотворение приводит к развитию нового живого организма еще большей сложности. 2) различия между гаметами и эмбрионом заключаются скорее в степени (сложности), чем в принципе (их построения);оплодотворение не создает крутой перемены, вынуждающей приписывать абсолютную ценность или безусловное право (например, на жизнь) яйцеклетки от момента оплодотворения. 3) проэмбрион заслуживает защиты, которая не подразумевает абсолютного права на жизнь. 4) эмбрион имеет право на жизнь, но это право может быть отвергнуто при определенных, но строго аргументированных ситуациях (поздние аборты и пр.). 5) этически приемлемы исследования in vitro на эмбрионах до 14-го дня после оплодотворения [45]. Кратко рассмотрим аргументы в пользу этой градуалистической релятивистской позиции, сформулированные в докладе профессора G. Hermeren [45]: физиологические — преэмбрион не имеет мозга и нервной системы, никаких характеристик личности: самосознания, рациональности, чувства морали, автономии и т.д; психологические — способность чувствовать удовольствие и боль, внешний вид и свойства, возможности развиваются у эмбриона (плода) постепенно. Индивидуальность — оплодотворение еще не означает становление индивидуальности, из зиготы могут развиться несколько индивидуумов. По каким критериям можно утверждать, что оплодотворенная яйцеклетка и рожденный (из нее) ребенок — один и тот же индивидуум? Вероятность становления новой личности очень мала в силу большого числа внедряющихся в этот процесс ситуаций, и она снижается по мере прогрессирования развития. В силу прогресса знаний, в том числе биологических, могут меняться стандарты этических правил, в том числе относительно статуса эмбриона. Происходит последовательное снижение зависимости эмбриона от матери, определенное увеличение его автономности по мере прогрессии беременности. Аргумент преемственности — генетической, но с включением и выключением определенных звеньев (регуляции) и возможным возникновением мутаций. Аргумент генетический: вариации на генетическом уровне в аллелях или продуктах экспрессии генов усложняют определение сущности как генетически человеческого существа. Аргумент интересов — физиологических условий развития для эмбриона и плода, которые могут не совпадать с планами матери. ЭКО-аргументы: имеются важные различия между развитием эмбриона in vitro и in vivo, например, невозможность формирования первичной полоски in vitro. Научная ценность исследований на эмбрионах in vitro (до 14-го дня развития) несомненна и т.д.[ 45]. Эти и многие другие вопросы широко обсуждаются во многих странах. Проблемы биомедицинской этики в репродукции и, в первую очередь, о статусе эмбриона только начинают подниматься в нашей стране [12—15, 20, 53]. Широкое обсуждение с привлечением медиков и биологов, философов и социологов, юристов и теологов проблемы статуса эмбриона человека, проводимое в мире в последние годы (3d Symposium on Bioethics, Concil of Europe,1996; [40]) свидетельствует о сложности, противоречивости, на сегодня — неразрешимости вопроса об определении статуса эмбриона человека. Как отмечают, определение критериев морального статуса является философской проблемой. После этого встают эмпирическая и научная проблемы — какая стадия становления эмбриона человека соответствует этим критериям: генетическая, биологическая, личностная, интересов, возможностей? [45]. Остановить использование ВРТ невозможно по ряду причин, но накапливается информация об отрицательных моментах и необходимости большего контроля за медициной и охраной здоровья населения в целом. Это обсуждали на Всемирном конгрессе по биоэтике (1996), в 50-ю годовщину Нюрнбергского процесса над фашистами. Назрела необходимость всестороннего обсуждения и определения статуса эмбриона человека, создания соответствующих международных правил действенного лицензирования учреждений и специалистов, занимающихся в области ВРТ, в области биотехнологий, генной инженерии и проведения регулярного контроля за их работой со стороны независимых организаций. Необходимо расширить рамки морали и соблюдать основной тезис медицины «...Не навреди». Л.Ф. Курило Медико-генетический научный центр РАМН, Москва Литература 1. Астраханцев А.Ф. Структура мужских половых желез в постнатальном онтогенезе. Дисс. ... докт.мед.наук, Рязань,1996;294. 2. Брагина Е.Е., Курило Л.Ф., Шилейко Л.В. и др. Бесплодие при глобулозооспермии и отсутствие акросомы сперматозоидов. Пробл репрод 1997;3:3:53—55. 3. Брагина Е.Е., Курило Л.Ф., Шилейко Л.В. и др. Ультраструктурный и количественный кариологический анализ половых клеток из эякулята пациента с абсолютной астенозооспермией. Пробл репрод 1997;3:4: 72—75. 4. Великий П.Л., Шаповалов Ю.М. Яйцеклетка человека на стадии слияния пронуклеусов, оплодотворенная в естественных условиях. Арх анат 1981;80: 6: 81—82. 5. Заварзин А.А. Краткое руководство по эмбриологии человека и позвоночных животных. Наркомздрав, Ленинград 1939;204. 6. Конюхов Б.В. Клонирование позвоночных: успехи и проблемы. Генетика 1997;33:12:1605—1620. 7. Кулешов Н.П., Бочков Н.П., Алехин В.И. и соавт. Цитогенетическое исследование 6000 новорожденных детей. Генетика 1978;14:2:340—347. 8. Красовская О.В. Оплодотворение яйца кролика in vitro. Архив анат 1934;13:2:327—342. 9. Курило Л.Ф. Динамика преобразований хромосом в профазе I мейоза в оогенезе человека. Цитология 1980 а;22:24:154—160. 10. Курило Л.Ф. Развитие яичников человека в пренатальный период. Арх анат 1980 б;79:7:73—79. 11. Курило Л.Ф. Морфофункциональные характеристики оогенеза человека и млекопитающих. Дисс. ... докт. биол.наук, М 1985;470. 12. Курило Л.Ф., Гаева Т.Н., Шилейко Л.В. и соавт. Анализ результатов анкетирования по некоторым вопросам репродуктивных технологий. Пробл репрод 1996;2:1:29—36. 13. Курило Л.Ф. Право родиться. Человек 1995;4:112—119. 14. Курило Л.Ф. Некоторые морально-этические проблемы репродукции человека.151-171/ Кн.:Биомедицинская этика. Ред. В.И.Покровский. М.: Медицина, 1997;223. 15. Лопухин Ю.М. Биоэтика. Вестн. РАМН 1993;9 41—47. 16. Райцина С.С. Сперматогенез и структурные основы его регуляции. Москва, Наука 1985;206. 17. Семенова-Тян-Шанская А.Г. Первичные половые клетки зародыша человека в период миграции к зачаткам гонад. Арх анат 1969;56:6:3—8. 18. Фалuн Л.И. Эмбриология человека. Атлас. Москва, Медицина 1976; 544. 19. Хилькевич Л.В., Курило Л.Ф. Кинетика популяции мужских половых клеток человека в антенатальном периоде онтогенеза. Онтогенез 1992;23:5: 506—510. 20. Юдин Б.Г. Ред. Предисловие. В реф.сб. Проблемы биоэтики.М 1993; 5—17. 21. Baird D.T. Biological data, medical indications and statutory aspects of assisted conception. Report - Council of Europe’s Third Symposium on Bioethics 1996;Strasbourg. 22. Baker T.G. A quantitative and cytological study of germ cells in human ovaries. Proc.R.Soc.Lond.(Biol.) 1963;158:417—433. 23. Bodemer Ch.W. Modern embryology N.Y.,1968;475. 24. Boubakeur D. The embryo in Islam. Report — Council of Europe’s Third Symposium on Bioethics 1996; Strasbourg. 25. Bouй F., Boyй A., Lazar P. Retrospective and prospective epidemiological studies of 1500 karyotyped spontaneous human abortions. Teratology 1975;12: 11—26. 26. Byrne J.,Warburton D., Klein J., Blanc W., Stein Z. Morphology of early fetal death and their chromosomal characteristics. Teratology 1985;32:2:297—315. 27. Бодемер Ч. Современная эмбриология, Изд. «Мир», Москва, 1971;6:446. 28. Chia C.M., Winston R.M.L., Handyside A.H. EGF,TFG-& and EFGR expression in human preimplantation embrios. Development 1995;121:2: 299—307. 29. Chiquoine A.D. Observation on the early events of cadmium necrosis of the testis. Anat Rec 1964;149: 23—36. 30. Corliss C.E. Patten’s human embryology.Elements of clinical development. McGroww-Hill Book Company, A Blackiston Publication, N.Y., a.o.,1976;470. 31. Cross P.K. Cell mutations: rates and associated factors (New York state chromosome registry) Dir.On-Going Res Cancer Epidemiol.1989-1990/JARS/DRFZ-Lyon.1989;466—467. 32. Dale B., Gualtieri R., Talevi R., Tosti E., Satella L., Elder K. Intercellular communication in the early human embryo. Mol Reprod and Dev 1991;29:1:22—28. 33. Dickson D. British government rekindles debate on embryo research. Nature 1987;238:4832:1348. 34. Dvorak M., Tesarik J., Pilka L., Travnik P. Fine structure of human two-cell ova fertilized and cleaved in vitro. Fertil Steril 1982;37:5:6:661—667. 35. Edwards R.G. Causes of early embryonic loss in human pregnancy. Hum Reprod 1986;1:3:185—198. 36. Edwards R.G. Sciense et ethique de la segmentation des embrions humains in vitro. Contracpt. Fertil Sex 1986;14:4:313—318. 37. Edwards R.G. New ethical implications of human embryology. Hum Reprod 1986;1:4:277—278. 38. Egozcue J. Origin of Embryos used in research and what happens to them. Report - Council of Europe’s Third Symposium on Bioethics 1996; Strasbourg. 39. England M.A. Farbatlas der Embriologie F.K.Shattaner Verlag.- Stuttgart-N.Y.1985;25. 40. Evans D. Pro-attitudes to pre-embryos. In: Conceiving Embryo. Martinus Nijholff Publ., The Hague, Boston 1996;358: 3—7. 41. Gil-Salom M. et al. Efficacy of intracytoplasmic sperm injection using testicular spermatozoa. Hum Reprod 1995;10/12:3166—3170. 42. Grillo J.M.,Vasserot M.,Gamerre M., Vitry G., Stahl A. Nucleonar changes in Human embryo during the preimplantation stage. Activation of ribosomal genes during the nucleogenesis. Biol cell 1991;3:201—209. 43. Globstein C. External human fertilisation. Sci Amer 1979;240: 6:33—43. 44. Handyside A., Kontogianni E.H., Hardy K. et al. Pregnancies from biopsied human preimplantation embryos sexed by Y-specific DNA amplification. Nature 1990;344:768—770. 45. Hermeren G. Nature and status of the embryo: Philosophical aspects. Report — Council of Europe’s Third Symposium on Bioethics 1996; Strasbourg. 46. Hertig A.T., Rock J., Adams E.C., Menkin M.C. Thirty-four fertilized ova, good, bad and indifferent, recovered from 210 women of known fertility. Pediatrics 1952;23:202. 47. Honnefelder L. Nature and status of the embryo: Philosophical aspects. Report — Council of Europe’s Third Symposium on Bioethics 1996; Strasbourg. 48. Human Fertilization and Embryology Authority 1996; 5th An. Report. 49. Gualtieri R., Santella L., Dale B. Tight junctions and cavitation in the human preembryo. Mol Reprod and Dev 1992;32:1:81—87. 50. Jacobs P.A. Chromosome mutations: frequency at birth in humans. Humangenetik 1972;16:1-2:137—139. 51. Knoppers B.M. Nature and status of the embryo: Legal aspects. Report — Council of Europe’s Third Symposium on Bioethics 1996; Strasbourg. 52. Kurilo L.F. Oogenesis in Antenatal Development in Man. Hum Genet 1981;57:1:86—92. 53. Kurilo L.F. Nature and status of the embryo: Scientific aspects. Report — Council of Europe’s Third Symposium on Bioethics 1996; Strasbourg. 54. Malter H., Talansky B., Gordon J. et al. Monospermy and polyspermy after partial zona dissection of reinseminated human oocytes. Gamete Res 1989;23:4:377—386. 55. Mancini R.E. Allergic aspermatogenesis experimental induced in man and animals. Jn: Intern.symp.on injurey, inflamation and immunity. Baltimore 1964;365—377. 56. Martin R.N., Balkan W., Burns K. et al.The chromosome constitution of 1000 human spermatozoa. Hum Genet 1983;63:2: 305—309. 57. McLaren A. IVF: regulation of prohibition? Nature 1989;342: 6249:469—470. 58. McLaren A. Research on embryos in vitro. The various types of research. Report - Council of Europe’s Third Symposium on Bioethics 1996; Strasbourg. 59. Miller J.F., Williamson E., Glue J.,Gordon J.B., Grudzinskas J.G., Sykes A. Fetal loss following implantation:a prospective study. Lancet 1980;8167:1:554. 60. Moore K.L. The Developing Human: Clinically oriented Embryology Philadelphia.,L, Saunders, 1973;374. 61. Muller F.O., O’Rahilly R. The first appearance of the neural tube and optic primordium in the human embryo at stage 10. Anat Embryol 1985;172:2:157—169. 62. Muller F.O., O’Rahilly R. The first appearance of the human nervous at stage 8. Anat and Embryol 1981;163:1:1—13. 63. Nadeau J.H., Dietz K., Tamarin R. Gametic selection and the selection component analysis. Genet Res 1981;37:3:276—284. 64. Noonan J.T. An Almost Absolute Value in History. In: J.T.Noonan, ed., The Morality of Abortion, Cambridge, Mass.: Harvard University Press 1970. 65. Orts-Llorca F. La somitogenese chez l’embryon humain: des myotomes. Bull Assoc anat 1981;65:191:467—482. 66. Palermo G., Joris H., Devroy P. et al. Pregnancies after intracytoplasmic injection of single spermatozoon into an oocyte. Lancet 1992;8810:17—18. 67. Patten B.M. Foundations of embryology. N.Y. 1958. 68. Patten B.V. Human Embryology. Re-edition. Maidenhead, McGraw Hill 1976. 69. Pembrey M.E. Pre-implantation diagnosis: Ethical aspects. Report — Council of Europe’s Third Symposium on Bioethics 1996; Strasbourg. 70. Pereda J., Crozatto H.B. Fine structure of an early human morula optained from the uterine cavity: Sci. Pap.Present. 46th Annu. Meet. Fertil. Soc., Washington, D.C., Oct.13—18,1990:Abstr. 1990;74:227:15—16. 71. Pereda J., Cheviakoff S., Croxtto H.B. Ultrastructure of a 4-cell human embryo developed in vivo. Hum Reprod 1989;4:6:680—688. 72. Pincus G. The maturation of explanted human ovarian ova. Amer J Physiol 1939,126:3600. 73. Plachot M. Pre-implantation diagnosis: Technical aspects. Report — Council of Europe’s Third Symposium on Bioethics 1996; Strasbourg. 74. Reinold E. Fetal motor behaviour during pregnancy as a dynamic criterion of embryo-fetal health. Invest. Ultrasonol. 2 Clin. Adv., London 1981;78—86. 75. Rock J., Menkin M. In vitro fertilization and cleavage of human ovarian eggs. Science 1944;100:1:105—108. 76. Steirteghem A. Van Selection of gametes and techniques for assisted fertilisation. Report — Council of Europe’s Third Symposium on Bioethics 1996; Strasbourg. 77. Steptoe P.C., Edwards R.G. Birth after reimplantation of a human embryo. Lancet 1978;2:366. 78. Speed R.M., Chandley A.C. Prophase of meiosis in human spermatocytes analysed by EM microspreading in infertile men and their controls and comparisons with human oocytes. Hum Genet 1990;84:6:547—554. 79. Tawia S. When is the capacity for sentence acquired during fetal development? J Maternal- Fetal Med 1992;1:3:153—165. 80. Warnock M. Report of the Committee of Inquiry into Human Fertilization and Embryology. HMSO.CMND.9314.1984. 81. Warnock M. Do Human cells have right? Bioethics 1985;1:1:1—14. 82. Wilmut I., Schnieke A.E., McWhir J. et al. Viable offspring derived from fetal and adult mammalian cells. Nature 27/2- 1997;385:810—813. От редакции. Авторы статьи “Эндокринное бесплодие у мужчин”, опубликованной в № 4/97, приносят свои извинения за отсутствие ссылки на работы, в которых приводимая в статье схема была опубликована ранее: Л.Ф. Курило и соавт. “Современные подходы к оценке состояния гаметогенеза и репродуктивной функции человека и млекопитающих”, Докл. на общ. цитологов, Москва, 1987. Цитол 1988;30:8:1027—1028.; Л.Ф. Курило и соавт. “Структура хромосомной патологии среди пациентов с нарушением репродуктивной системы” Тез. докл. Рос. съезда мед. генетиков. М 1994; 1: 85—86. |