Клинико-диагностическое значение определения фактора роста плаценты у беременных.
|
В последние годы большое внимание в мировой литературе уделяется факторам роста (ФР), являющихся биологически активными соединениями, стимулирующими или ингибирующими деление и дифференцировку различных клеток, в том числе контролирующими этот процесс c начальных этапов развития плаценты [1, 5, 6, 8, 9].
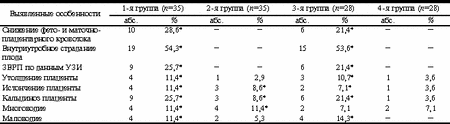
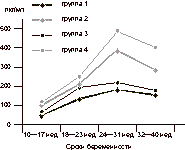
Используемые в настоящее время методы изучения состояния плода и фетоплацентарной системы в целом отражают различные аспекты ее функционирования, в связи с чем параллельное использование нескольких разнонаправленных методик повышает их информативность. Поиск новых методов ранней диагностики и прогнозирования хронической плацентарной недостаточности, оставаясь одним из приоритетных направлений современного акушерства, привел к необходимости использования определения факторов роста как ранних маркеров этой патологии [1, 7, 11]. На сегодняшний день установлено, что система плацентарных факторов роста регулирует рост и функцию сосудов плаценты. С одной стороны, они являются стимуляторами ангиогенеза и повышают проницаемость сосудов внутри плацентарного ложа, а с другой стороны, посредством аутокринного механизма регулируют инвазию, дифференцировку и метаболическую активность трофобласта в момент плацентации [5, 6, 8, 9]. Целью настоящего исследования явилась комплексная оценка состояния фетоплацентарного комплекса с обоснованием диагностической и прогности ческой значимости определения уровня фактора роста плаценты в сыворотке крови беременных. Материал и методы Был проведен анализ исходной клинической характеристики, особенностей течения беременности и родов, состояния плодов и новорожденных, а также уровня фактора роста плаценты (ФРП), щелочной фосфатазы (ЩФ) и плацентарной щелочной фосфатазы (ПЩФ) в сыворотке крови у 126 женщин. В зависимости от наличия у них признаков хронической плацентарной недостаточности (ХПН) и/или инфекции пациентки были разделены по группам. 1-я группа - 35 беременных с инфекцией и ХПН, 2-я группа - 35 беременных с различной инфекционной патологией без ХПН, 3-я группа - 28 беременных с ХПН без инфекции, группу контроля составили 28 женщин с неосложненным течением беременности - 4-я группа. Диагноз хронической плацентарной недостаточности устанавливался на основании комплексного динамического обследования. Основными критериями при постановке диагноза ХПН являлись: 1. Отставание роста плода по данным биометрии на >2 нед. 2. Снижение фето- и маточно-плацентарного кровотока при допплерометрии - С/Д a.uterinae >2,4, a.umbilicalis >3,2, a.cerebralis media <4,4. 3. Наличие признаков внутриутробного страдания плода при кардиотокографии - ПСП>1,0. Проводились общеклинические, лабораторные, функциональные методы исследования. Фетоплацентометрия осуществлялась с помощью ультразвуковых аппаратов "Aloka SSD-680" и "Toshiba-38A" (Япония). Мониторный контроль за состоянием плода в III триместре осуществлялся с помощью кардиотокографов 8030А фирмы "Hewlett-Packard" и МТ-801 фирмы "Toitu" (Япония). При анализе КТГ вычислялся показатель состояния плода (ПСП) по формуле, предложенной В.Н. Демидовым и соавт. Для оценки маточно-плацентарно-плодового кровотока производили допплерометрическое исследование с помощью приборов "Aloka" ССД-680 и "Aloka" ССД-2000 с использованием трансабдоминальных датчиков частотой 3,5 и 5,0 МГц в режиме пульсовой допплеров ской волны. Определение в сыворотке крови уровня фактора роста плаценты (ФРП) осуществлялось иммуноферментным методом с помощью наборов "P&D systems" (Великобритания), щелочной фосфатазы (ЩФ) и плацентарной щелочной фосфатазы (ПЩФ) - на биохимическом анализаторе "Ультра" производства фирмы "КОНЕ" (Финляндия) в стандартных условиях и использованием реагентов фирмы "КОНЕ". Все последы родившихся детей были направлены на морфологическое исследование. При этом применялись следующие методы: макроскопический, морфометрический, гистологический, иммуногистохимический. Статистическая обработка полученных результатов выполнялась с использованием пакета прикладных программ для статистической обработки "Excel" версия 7,0, раздел программы "Анализ данных". Различия между сравниваемыми величинами признавали статистически достоверными при уровне значимости р<0,05. Результаты и обсуждение Возраст беременных колебался от 19 до 40 лет и составил в среднем 28,2±1,1 года. При анализе массо-ростовых соотношений у обследованных женщин отклонений от популяционных норм не выявлено, средняя масса тела перед наступлением беременности - 68,4±1,9 кг, средний рост - 167,6±0,9 см. Наиболее часто встречающимися осложнениями гестационного периода были: угроза прерывания в I и II триместрах, гестоз, анемия, угроза преждевременных родов. В 1-й и 2-й группах отмечалось обострение хронических заболеваний мочевыделительной системы, острых респираторных вирусных и герпесвирусной инфекций (вирус простого герпеса и цитомегаловирус), хламидиоза. При применении функциональных методов исследования выявлены особенности, представленные в табл. 1. Данные, представленные в табл. 1, свидетельствуют о том, что признаки ХПН по данным функциональных методов исследования (задержка внутриутробного развития плода, снижение кровотока в сосудах системы мать-плацента-плод, хроническая внутриутробная гипоксия плода) встречались примерно с одинаковой частотой в 1-й и 3-й группах. Показатели метаболической активности плаценты представлены в табл. 2. Как видно из представленных данных, средний уровень ПЩФ у женщин 2-й группы был ниже, чем в контрольной группе, однако соотношение ПЩФ/ЩФ сохранялось в пределах нормы. В то время как в 1-й группе отмечалось достоверное снижение как уровня ПЩФ, так и показателя соотношения. В группе женщин, где ХПН не сочеталась с инфекцией, все средние показатели достоверно не отличались от показателей в группе контроля. Необходимо отметить, что наблюдались индивидуальные колебания показателей ЩФ и ПЩФ как в основных, так и в контрольной группах. Всем включенным в группы исследования пациенткам проводилось определение уровня ФРП, начиная с конца I триместра гестации (табл. 3, рис. 1). Как видно из данных, представленных в табл. 3 и рис. 1, при физиологическом течении беременности (4-я группа) к 10 нед гестации наблюдался резкий подъем уровня ФРП, имевший к концу I - началу II триместра средние значения - 126±12,2 пкг/мл, продолжавший неуклонно расти и достигавший своего пика к началу III триместра - 480±15,9 пкг/мл. В дальнейшем после 32 нед беременности наблюдалось некоторое снижение уровня ФРП, средние значения которого к концу периода гестации составили 394±14,3 пкг/мл. Содержание ФРП в периферической крови являлось маркером внутриутробных процессов плацентации, становления и развития плацентарного кровообращения, а также функционирования фетоплацентарного комплекса (ФПК) в целом [5, 6, 11]. Наиболее интенсивный рост ворсин хориона и увеличение размеров плаценты, происходящее в I и II триместрах гестации, сопровождалось прогрессивным увеличением ФРП, достигавшим своего пика примерно к 28 нед гестации - сроку, в котором завершается 90% всего внутриутробного процесса роста [1, 4]. Данные, приведенные в табл. 3 и рис. 1, показывают, что у беременных 1-й и 3-й групп (с развившейся плацентарной недостаточностью) отмечалась неадекватная продукция ФРП с начала беременности. Уровень исследуемого фактора у этих пациенток оставался резко сниженным в течении всего периода гестации, достоверно отличаясь от группы контроля. У женщин 2-й группы (с активацией инфекционного процесса без клинической манифестации ПН) показатели ФРП также были достоверно ниже, чем в группе контроля во всех исследуемых точках, однако отклонения не были столь резко выражены и были достоверно выше, чем в 1-й и 3-й группах. Таблица 1. Результаты обследования беременных
Примечание. * - достоверные различия между группами (р<0,05). Таблица 2.Показатели ЩФ, ПЩФ и их соотношения в сыворотке крови беременных (M±m)
Примечание. * - достоверные различия между группами (р<0,05). Таблица 3. Уровень фактора роста плаценты (пкг/мл) в крови у обследуемых беременных (M±>m)
* - достоверные различия с группой контроля (р) (р<0,05); - достоверные различия с группой сравнения (р) (р<0,05); ** - достоверные различия с группой сравнения (р) (р<0,05).
Уровень фактора роста плаценты (пкг/мл) в крови у обследованных беременных. Всего у беременных произошло 126 родов. Частота преждевременных родов у пациенток 1-й группы составила 31,4%, что более чем в 2 раза превышало данную частоту в 3-й и 2-й группах (соответственно 15,4 и 11,4%). В 4-й группе все роды были своевременными. Исход родов для плода и течение раннего неонатального периода проанализированы у 127 детей (в 2 случаях в 1-й группе - двойни). Масса доношенных новорожденных колебалась от 2850 до 3900 г и составила в среднем 3445±121 г, недоношенных - от 1100 до 2350 г - в среднем 1844±77 г. Наибольший процент недоношенных детей встречался в 1-й группе и составил 35,1% (в 3-й группе - 15,4%, во 2-й группе - 11,4%). Кроме того, в одном случае в 1-й группе имела место антенатальная гибель плода. Клинические признаки гипотрофии новорожденного отмечались в 14,3% в 3-й группе, в 5,3% - во 2-й группе и в 34,3% - в 1-й группе, а в 4-й группе гипотрофии новорожденных не было. Следует отметить, что в 1-й группе в 1 случае имела место выраженная гипотрофия III степени. Внутриутробное инфицирование плода с наибольшей частотой встречалось в 1-й группе (40,0%), что почти в 2,5 раза превышало частоту данной патологии во 2-й группе (17,1%) (р<0,01). В 3-й и 4-й группах внутриутробного инфицирования плода не было. Во всех случаях поставленный клинически диагноз ХПН, был подтвержден при морфологическом исследовании последа. ХПН характеризовалась: патологической незрелостью плаценты, выражающейся в диссоциированном развитии ворсинчатого хориона, наличием инволютивно-дистрофических процессов и циркуляторных расстройств. В последах женщин, беременность которых протекала с признаками ХПН, но родившие детей без гипотрофии, патологические изменения сочетались с хорошо выраженными компенсаторно-приспособительными процессами. На конечном этапе исследования было проведено сопоставление и сравнительная оценка результатов всего комплекса обследования, оценивавших ФПК с начала беременности клинически, функционально, а также на уровне процессов метаболизма и клеточной регуляции. Выявлено, что во всех случаях в 1-3-й группах при наличии признаков задержки внутриутробного развития плода и гипотрофии новорожденного уровень ФРП не достигал нормативных значений во всех триместрах гестации (см. табл. 3), ПЩФ был ниже 123,2 Ед/л (N=123,2-151,8 Ед/л), а соотношение ПЩФ/ЩФ ниже 0,44 (N=0,44-0,50) (см. табл. 2). В 1-й группе на фоне стабильно низкого уровня ФРП имело место снижение ПЩФ и ПЩФ/ЩФ в 14,3%, и во всех этих случаях дети родились с признаками гипотрофии. Во 2-й группе в одном случае имело место прогрессивное снижение ФРП с 31 нед до 174 пкг/мл, сопровождавшееся сначала повышением ПЩФ до 152 Ед/л, а затем резким снижением ее уровня в 35 нед до 4 Ед/л и ПЩФ/ЩФ до 0,03. Признаков ХПН по данным функциональных методов исследования не наблюдалось, однако ребенок родился с гипотрофией II степени и явлениями внутриутробного инфицирования. Наибольший процент изменений со стороны исследуемых показателей имел место в 1-й группе. В случае антенатальной гибели плода кривая нарастания ФРП не имела выраженного подъема как при физиологической беременности, а характеризовалась плавным подъемом к 28-30 нед не достигающим показателей нормы, а затем более крутым падением уровня исследуемого фактора, достигшим за 2 нед до гибели плода минимальных значений для III триместра (47 пкг/мл), показатель ПЩФ при этом был равен нулю. В 2 случаях имело место резкое падение уровня ФРП в начале III триместра до 120 пкг/мл с последующим снижением ПЩФ до 2 Ед/л и соотношения ПЩФ/ЩФ соответственно до 0,01 и 0,02. В первом случае ребенок родился с гипотрофией III степени, во втором с гипотрофией II степени и генерализованной внутриутробной инфекцией. По данным функциональных методов исследования в обоих случаях имели место ЗВРП по данным УЗИ, снижение фето- и маточно-плацентарного кровотока по данным допплерометрии и выраженные признаки внутриутробного страдания плода при кардиомониторном исследовании, диагностированные в III триместре. Во всех остальных случаях у женщин, родивших детей с признаками гипотрофии, имело место снижение уровня ПЩФ и соотношения ПЩФ/ЩФ. Кривые нарастания ФРП в этих случаях также не имели характерного крутого подъема, а уровень его начинал достоверно снижаться примерно за 2 нед до начала метаболических изменений в плаценте и падении уровня ПЩФ и за 3-4 нед до клинической манифеста ции ПН, диагностируемой при помощи функциональ ных методов исследования. Высокий процент повышения уровня ПЩФ в 1-3-й группах являлся результатом адаптационной гиперферментемии и наблюдался при начальных признаках нарушений в фетоплацентарной системе, что согласуется с литературными данными [2, 11]. Это свидетельствовало о том, что энергетический обмен в ткани плаценты при нарушении состояния плода характеризовался на первом этапе усилением биосинтетических процессов, а в последующем снижением их интенсивности. Метаболические изменения в плаценте сопровождались соответственно сначала повышением активности ПЩФ в сыворотке крови и характеризовали начальные признаки нарушений в системе мать-плацента-плод, а затем снижением ее активности, что являлось неблагоприятным прогностическим признаком для плода и новорожденного и согласует ся с ранее проведенными исследованиями [2]. Анализ проведенной работы подтвердил последние литературные данные [1, 6, 9], указывающие на сложную цепочку процессов, последовательно происходящих в плаценте и регулируемых факторами роста. При физиологически протекающей беременности продукция ФРП начинается с 8-10 нед гестации и характеризуется резким его нарастанием, достигающим максимальных значений к 28-30 нед, а затем незначительным падением данного показателя. У женщин с патологическим течением гестационого процесса в 92,5% случаев имеет место нарушение продукции ФРП с начала беременности, характеризующееся достоверно более низкими значениями его показателей за время всего периода гестации, отсутствием крутого подъема кривой его нарастания в течении I-II триместров и выраженного пика максимальных значений к 28 нед. Нарушение функциональной активности ФРП с выраженным падением его значений в периферической крови начинается за 2-3 нед до начала метаболических нарушений плаценты с изменением ферментативной активности крови, характеризующееся вначале адаптационной гиперферментемией, а затем фазой истощения и падением показателей ПЩФ, а также коэффициента соотношения ЩФ/ПЩФ. Клиническая манифестация ПН с изменениями со стороны функциональных методов возникает через 4-5 нед после нарушения процессов клеточной регуляции и через 1-2 нед после изменения метаболизма плаценты. При начальных проявлениях или компенсированной форме плацентарной недостаточности показатели клеточной регуляции и ферментативной активности могут являться единственными маркерами начинающегося патологического процесса, что подтверждается в дальнейшем морфологической диагности кой и неблагоприятными перинатальными исходами. Результаты наших исследований согласуются с литературными данными [3, 4] о несомненной роли инфекции как отягощающего фактора в течении беременности, развитии ХПН и исходе родов. Неблагоприятный фон, обусловленный инфекцией, оказывает отрицательное влияние на адекватную продукцию и функционирование ФР, метаболизм плаценты и ее способность в развитии необходимых адаптационных реакций [2, 3, 10, 11]. У пациенток с активацией инфекционного процесса, не получавших адекватной терапии, имели место наиболее выраженные изменения со стороны продукции ФРП, ферментативной активности крови, отмечалась высокая частота рождения недоношенных и маловесных детей, перинатальной заболеваемости, что согласуется с имеющимися литературными данными [2, 3, 8]. Таким образом, уровень ФРП является ранним прогностическим маркером, характеризующим начальные признаки нарушений в ФПК, возникающие задолго до клинической манифестации ХПН. Все вышеизложенное свидетельствует о том, что понимание механизмов действия системы факторов роста способствует появлению новых эффективных методов прогнозирования и ранней диагностики синдрома ХПН, что послужит реальным резервом снижения перинатальной заболеваемости и смертности, особенно у беременных группы высокого риска, в том числе с инфекцией. В.А. Бурлев, З.С. Зайдиева, В.Л. Тютюнник Научный центр акушерства, гинекологии и перинатологии РАМН, Москва Литература 1. Бурлев В.А., Зайдиева З.С., Тютюнник В.Л., Кравченко Н.Ф., Павлович С.В., Коноводова Е.Н. Роль факторов роста в развитии плацентарной недостаточности. Пробл репрод 1999; 5: 6: 7-12. 2. Бурлев В.А., Зайдиева З.С., Тютюнник В.Л., Лапшина И.И. Клинико-диагностическое значение плацентарной щелочной фосфатазы у беременных при хронической плацентарной недостаточности и инфекции. Пробл репрод 2000; 6: 5: 56-60. 3. Орджоникидзе Н.В., Тютюнник В.Л. Хроническая плацентарная недостаточность при бактериальной и/или вирусной инфекции. Акуш и гин 1999; 4: 46-50. 4. Савельева Г.М., Федорова М.В., Клименко П.А., Сичинава Л.Г. Плацентарная недостаточность. М: Медицина 1991; 272. 5. Athannassiades A., Lala P.K. Role of placenta growth factor (PLGF) in human extravillious trophoblast proliferation, migration and invasiveness. Placenta 1998; 19: 7: 465-473. 6. Hill D.J., Petrik J., Arany E. Growth factors and the regulation of fetal growth. Obstеt Gynecol 1998; 92: 2: 179-183. 7. Khaliq A., Li X.F., Shams M., Sisi P., Acevedo C.A., Whittle M.J., Weich H., Ahmed A. Localization of placenta growth factor (PLGF) in human term placenta. Growth Factors 1996; 13: 243-250. 8. Lala P.K., Lysiak J.J. Autocrine-paracrine regulation of human placental growth and invasion by locally active growth factors. (Ed. Kurpisz M., Fernandes N.) Immunol Hum Reprod 1995; 235-249. 9. Li R.H., Zhuang L.Z., Hum U.Z. The effects of growth factors on human normal placental cytotrophoblast cell proliferation. Reprod 1997; 12: 4: 830-834. 10. Okesina A.B., Donaldson B., Lacelles P.T., Moris P. Effect of gestational age on levels of serum alkaline phosphatase isoenzymes in healthy pregnant women. Obstet Gynec 1995; 48: 1: 25-29. 11. Shore V.N., Wang T.N., Wang T.L., Torry R.G., Caudle M.R., Torry D.S. Vascular endotelial growth factor, placenta growth factor and their receptors in isolated human trophoblast. Placenta 1997; 18: 657-669. |