Возможность использования бета-каротина в качестве лечебно-профилактического средства.
|
Проблема воздействия производственной среды на репродуктивную функцию мужчин является весьма актуальной в связи с появлением многочисленных сведений о существенной роли токсических агентов в развитии мужской субфертильности и бесплодия, индуцировании мутаций в мужских половых клетках, которые могут передаваться последующим поколениям, отягощая генофонд популяции, или приводить к развитию патологической беременности, спонтанным абортам, врожденным порокам развития [21, 23]. Особенно настораживают эпидемиологические исследования о существовании взаимосвязи между профессиональной занятостью отцов в ряде отраслей промышленности и развитием детских онкологических заболеваний [17, 18].
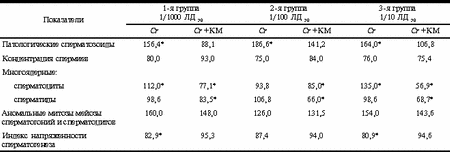
Исследования и свидетельства о гонадотоксичности и генотоксичности солей тяжелых металлов имеют давнюю историю. Еще в XIX в. врачи обратили внимание на высокую частоту бесплодия, спонтанных абортов, мертворождений, макро- и микроэнцефалий у новорожденных в семьях, где мужья работали на добыче и переработке соединений свинца [20]. В настоящее время установлено, что токсичность этой группы соединений напрямую зависит от их растворимости, валентности; продолжительности, дозы и путей поступления в организм; токсикокинетики и токсикодинамики; присущих им свойств ксенобиотика или микроэлемента; способности образовывать в организме промежуточные продукты; сродства к лигандам, белкам и т.д. [16]. В репродуктивной токсикологии накопилось достаточное количество эпидемиологических, экспериментальных и клинических наблюдений, позволяющих оценить особенности токсического действия металлов в области мужской репродукции, спрогнозировать риск развития специфической патологии и отдаленных последствий, разработать систему профилактических мероприятий на производстве [19]. Соединения шестивалентного хрома относятся к опасным загрязнителям производственной и окружающей среды, обладающими мутагенными, канцерогенными свойствами, и входят в перечень потенциально опасных химических веществ по действию на репродуктивную функцию человека [3, 7, 10]. Известно [10], что хром (VI) не встречается в природных условиях (являясь ксенобиотиком), соли этого соединения получают из хромовой руды на специализированных химических производствах, где они, практически, являются монофакторными токсическими загрязнителями, однако широко используются в ряде отраслей промышленности: металлургической, металлообрабатывающей, кожевенной, текстильной, химической и т.д. Кроме того, соединения шестивалентного хрома образуются при электросварке [10]. Ранее [1] специалистами НИИ охраны материнства и младенчества было проведено углубленное андрологическое обследование рабочих-аппаратчиков НПО «Хромпик» в динамике 4 сперматогенных циклов (ежеквартально в течение года), которое показало, что увеличение продолжительности контакта с соединениями хрома приводит к изменениям показателей подвижности мужских гамет в эякуляте, морфологии (увеличение доли аномальных клеток). В дальнейшем гонадотоксичность хрома была подтверждена в тест-системе in vitro на мужских гаметах и в нескольких сериях экспериментальных исследований на лабораторных животных [2, 11, 22]. Так, у самцов крыс линии Вистар был выявлен прямой токсический и мутагенный эффект на гонады при внутрибрюшинном поступлении бихромата калия в течение уже одного сперматогенного цикла в большом диапазоне доз (1/10, 1/100 и 1/1000 от ЛД 50), сопоставимых с воздействиями в производственных условиях. При этом при скрещивании подопытных самцов с интактными самками зарегистрировано значительное увеличение общей эмбриональной, доимплантационной и постимплантационной гибели плодов по сравнению с контрольной группой животных. Кроме того, в аналогичных условиях эксперимента установлено, что одним из возможных механизмов гонадотоксичности шестивалентного хрома является активация процессов перекисного окисления липидов и подавление систем антиоксидантной защиты в тканях семенников [12]. Одной из актуальных задач профилактической медицины в области репродуктивной токсикологии является поиск и внедрение в структуру лечебно-профилактического питания средств специфической и неспецифической профилактики развития профессионально обусловленной патологии. К перспективной группе препаратов, обладающих подтвержденными мембранопротекторными, антиоксидантными и антимутагенными свойствами, относятся каротиноиды, в частности, бета-каротин [9, 13]. Широкое применение нашел отечественный препарат «Каротин микробиологический (провитамин А) в масле», получаемый многократной экстракцией из сухой биомассы мукорового гриба Blakeslae trispora на химико-фармацевтическом объединении «Уралсинтез» (г. Екатеринбург). Кроме каротина в нем содержатся также токоферол, ненасыщенные жирные кислоты, 17 аминокислот, витамины группы В и другие биологически активные соединения [6]. Целью настоящей работы явилось исследование гонадопротекторных свойств препарата «Каротин микробиологический (провитамин А) в масле» при экспериментально вызванной хромовой интоксикации. Материал и методы Эксперименты проводились на половозрелых крысах разведения Вистар обоего пола. Моделирование хромовой интоксикации осуществлялось у трех групп самцов при ежедневном внутрибрюшинном введении бихромата калия (K2 Cr2 O7) на протяжении величины сперматогенного цикла (48-50 дней) в диапазоне доз кратным от ЛД 50: 1/1000 (1-я группа животных), 1/100 (2-я группа) и 1/10 (3-я группа), что составляет 0,028; 0,28; 2,8 мг/кг массы тела по веществу. Условия моделирования интоксикации соответствовали таковым в предыдущих сериях экспериментов, выявивших гонадотоксический и мутагенный эффекты у шестивалентного хрома [11]. «Каротин микробиологический (провитамин А) в масле» (в дальнейшем КМ) вводили 50% самцов крыс каждой группы перорально через зонд три раза в неделю в суточной дозе 2,8 мг, соответствующей по литературным данным противоопухолевому эффекту препарата у лабораторных грызунов [8]. Животным контрольной группы вводили внутрибрюшинно физиологический раствор или перорально подсолнечное масло в тех же объемах, что подопытным животным. В конце экспозиционного периода часть подопытных самцов спаривалась с интактными самками (в соотношении 1 самец + 2 самки) с последующим анализом эмбрионального материала, другая часть умерщвлялась методом декапитации для оценки морфофункционального состояния семенников в соответствии с методическими рекомендациями по этому вопросу [5, 16]. Так, в суспензии из хвостовой части эпидидимуса исследовали общее количество сперматозоидов и их осмотическую резистентность, процент подвижных клеток и клеток с аномальной головкой и хвостом. В мазках из гомогената семенников изучали следующие параметры: процентное соотношение всех типов половых клеток, клеток Сертоли и клеток Лейдига с расчетом индекса напряженности сперматогенеза (отношения всех половых клеток к сумме клеток Сертоли); процент многоядерных сперматогенных клеток; процент сперматид с микроядрами; количество митозов и мейозов на 1000 половых клеток (т.н. митотический и мейотический индексы) и наличие аномальных митозов и мейозов. У самок на 19-20-й день беременности анализировали эмбриональный материал: количество желтых тел беременности в яичниках; количество живых и мертвых эмбрионов; мест имплантаций и резорбций. Рассчитывались показатели общей эмбриональной, до- и постимплантационной гибели плодов. Статистическую обработку данных эксперимента проводили в зависимости от вида показателя с использованием критерия Стьюдента или непараметрических методов: U-критерий Вилкоксона-Манна-Уитни и критерий c2. Результаты и обсуждение В табл. 1, 2 указаны некоторые параметры сперматогенеза затравленных самцов и результаты исследования эмбрионального материала при их скрещивании с интактными самками после воздействия различных доз шестивалентного хрома. Таблица 1. Некоторые показатели состояния сперматогенного эпителия у подопытных животных в процентах по отношению к контролю (величина показателей в контрольной группе животных принята за 100%)
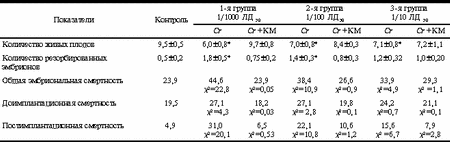
* - различия достоверны с контролем (р<0,05). Таблица 2. Результаты скрещивания опытных самцов с интактными самками
* - различия достоверны с контролем при р<0,05 и при c 2 >3,8. Анализ полученных результатов показал, что общие закономерности изменений показателей репродуктивной функции подопытных животных при хромовой интоксикации в условиях данного эксперимента соответствуют таковым в предыдущих сериях опытов [11]. Так, при исследовании эпидидимальных сперматозоидов отмечается тенденция к снижению общей концентрации клеток и статистически значимое увеличение морфологически аномальных форм во всех подопытных группах (табл. 1). В мазках из гомогената семенников - уменьшение общей популяции герминативных клеток в семенных канальцах; изменение процессов деления и дифференцировки клеток, отражающиеся в увеличении количества аберрантных митозов и мейозов, доли многоядерных половых клеток и сперматид, содержащих микроядра. Изучение эмбрионального материала от интактных самок после скрещивания с «затравленными» самцами свидетельствует о снижении процента беременностей и количества живых плодов; увеличении резорбированных эмбрионов, показателей общей эмбриональной, доимплантационной и, особенно, постимплантационной гибели во всех исследуемых группах животных по отношению к контролю (табл. 2). Учитывая, что постимплантационная гибель плодов, по мнению ряда авторов [4], отражает наличие доминантных летальных мутаций в гаметах и зиготах, можно предположить риск индукции подобных мутаций у мужчин-рабочих на производстве. Тем более, что соединения шестивалентного хрома способны вызывать в клетках хромосомные и хроматидные аберрации, однонитевые разрывы ДНК, генные мутации и ингибировать репаративный синтез ДНК [14]. Отсутствие дозоэффектной зависимости в эксперименте по этим показателям, характерное для мутагенов, лишь подтверждает такое предположение.
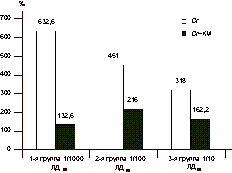
Рис. 1. Показатели постимплантационной гибели плодов после скрещивания самцов с воздействием хрома (Cr) и на фоне поступления каротина (Cr+KM). В процентах по отношению к величине показателя в контрольной группе, принятой за 100%.
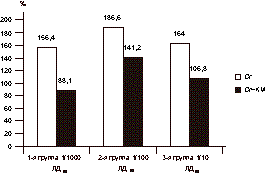
Рис. 2. Морфологически аномальные сперматозоиды в эпидидимусе крыс с воздействием хрома (Сr) и на фоне поступления каротина (Cr+KM). В процентах по отношению к величине показателя в контрольной группе, принятой за 100%. В совокупности полученные результаты эксперимента при хромовой интоксикации, по-видимому, отражают прямое токсическое и мутагенное действие металла на гонады самцов и/или опосредованное - путем известной для этих соединений способности образовывать активные метаболиты кислорода в тканях при взаимодействии с клеточными мембранами [12]. Последствия хромовой интоксикации у самцов крыс на фоне поступления в организм «Каротина микробиологического в масле» приобрели определенные изменения. При сохранившейся общей тенденции и направленности сдвигов большинства исследуемых показателей (табл. 1) в ряде случаев регистрировался эффект, расцененный нами как гонадопротекторный. Так, на фоне введения бета-каротина отмечается снижение процента многоядерных сперматогенных клеток не только по отношению к группам крыс с хромовой интоксикацией, но и по отношению к спонтанному уровню в контрольной группе животных; а содержание морфологически аномальных сперматозоидов в эпидидимусе снижается до уровня «контрольных» значений (табл. 1). Вместе с тем поступление каротина практически не отразилось на количественных показателях сперматогенного эпителия, пролиферативной активности тестикулярной ткани и концентрации сперматозоидов у подопытных самцов. Учитывая цель проведения эксперимента, наибольшего внимания заслуживают результаты скрещивания подопытных самцов с интактными самками (табл. 2). Можно предположить, что поступление препарата КМ нормализует фертильность особей с хромовой интоксикацией: процент беременных самок и количество живых плодов соответствуют таковым в контрольной группе животных. Анализ эмбрионального материала показывает, что на фоне действия бета-каротина нивелируется патологический эффект шестивалентного хрома на процессы имплантации-резорбции плодов и эмбриональной смертности. Наиболее выраженное действие каротина микробиологического наблюдается по показателю постимплантационной гибели плодов (табл. 2), которое возможно отражает антимутагенные и гонадопротекторные свойства исследуемого препарата при хромовой экспозиции у самцов в условиях данного эксперимента. Таким образом, полученные результаты исследования свидетельствуют, что поступление препарата «Каротин микробиологический в масле» замедляет развитие патологических процессов в тканях гонад и способствует нормализации показателей репродуктивной функции самцов крыс с хромовой интоксикацией. С учетом известных антиоксидантных, мембраностабилизирующих, антимутагенных свойств каротина микробиологического, можно рекомендовать его применение в качестве эффективной биодобавки в структуре лечебно-профилактического питания в условиях соответствующих производств и в рационе населения территорий, загрязненных солями тяжелых металлов. Л.Д. Шейко, В.П. Мамина, С.Л. Балезин Уральский НИИ охраны материнства и младенчества Минздрава России, Институт экологии растений и животных Уральского отделения РАН, Центр семейной медицины, Екатеринбург Литература 1. Балезин С.Л., Шейко Л.Д., Чистякова Г.Н. и др. Клинико-лабораторная диагностика нарушений репродуктивной функции мужчин (на примере рабочих, контактирующих с соединениями хрома). Актуальные проблемы репродукции семьи. Сб. науч. трудов. Екатеринбург 1997; 111-119. 2. Балезин С.Л., Шейко Л.Д. Использование суспензии сперматозоидов человека для биологического тестирования токсических загрязнителей внешней среды. Актуальные проблемы репродукции семьи. Сб. науч. трудов. Екатеринбург 1997; 137. 3. Гигиенические требования к условиям труда женщин: Санитарные правила и нормы 2.2.0.555-96. М 1997; 35. 4. Гигиенические критерии состояния окружающей среды. Руководство по краткосрочным тестам для выявления мутагенных и канцерогенных химических веществ. ВОЗ. Женева 1989; 109-135. 5. Методические рекомендации «Методы экспериментального исследования по установлению порогов действия промышленных ядов на генеративную функцию с целью гигиенического нормирования». М 1978. 6. Муравьева И.А., Ковальская Г.И. Физико-химические свойства и биологически активные вещества препарата «Каротин микробиологический в масле». Фармация 1988; 3: 32-35. 7. Перечень веществ, продуктов, производственных процессов, бытовых и природных факторов, канцерогенных для человека. Федеральные санитарные правила, нормы и гигиенические нормативы. ГН 1.1.029-95. М 1995; 3-7. 8. Потехина Н.И., Коломийцева И.К., Жарикова А.Д. Влияние бета-каротина на липиды цитоплазматических мембран клеток крыс при хроническом гамма-облучении. Бюллетень экспериментальной биологии и медицины 1993; 10: 370-373. 9. Сергеев А.В., Вакулова Л.Ф., Шашкина М.Я. и др. Медико-биологические аспекты каротиноидов. Вопросы медицинской химии 1992; 6: 8-11. 10. Хром. Гигиенические критерии состояния окружающей среды. Выпуск 61. ВОЗ, Женева 1990. 11. Шейко Л.Д., Мамина В.П. Действие шестивалентного хрома на сперматогенный эпителий и процессы перекисно го окисления липидов в гонадах лабораторных животных. Санитария и Гигиена 1997; 5: 487-489. 12. Шейко Л.Д., Чарушникова Г.А., Мамина В.П. Интенсивность процессов перекисного окисления липидов в гонадах как индикатор ранних изменений в репродуктивной системе мелких млекопитающих. Экология 1998; 6: 487-488. 13. Шлянкевич М.А., Дризе О.Б., Хабибулина В.М. и др. Антимутагенные свойства препаратов, содержащих бета-каротин. Вопросы медицинской химии 1992; 6: 23-25. 14. Baker R., Barm-David G., Bonin A. et al. Chemistry, biochemistry and mutagenicity of chromium (VI). J Inorg Bioch 1991; 2: 3: 466. 15. Chapin R., Heidel J. Male reproductive toxicology. London 1993; 371. 16. Clarkson T., Friberg L., Nordberg G. eds. Biological monitoring of toxic metals. NY 1988. 17. Gold E., Deiner M., Szklo T. Parental occupations and cancer in children. J Occup Med 1982; 24: 578-584. 18. Kwa S., Fine L. The association between parental occupation and childhood malignancy. J Occup Med 1980; 22: 792-794. 19. Miller R., Bellinger D. Metals. Occupational and environmental reproductive hazards. Baltimore 1996; 2. 20. National Research Council. Biomarkers of toxicity during reproduction and development. Washington 1989. 21. Scialli A., Zinaman M. Reproductive toxicology and Infertility. McGraw-Hill, Inc. 1993; 338. 22. Sheyko L.D., Balezin S.L. Morphostructural changes in rat gonads from hexavalent chromium. Reprod Toxicol 1993; 7: 5: 525. 23. Wyrobek A. Male biomarkers of abnormal reproductive outcome. Health Environ Digest 1990; 4: 1-4. В издательстве МедПресс вышло «Руководство ВОЗ по исследованию спермы и взаимодействию спермы с цервикальной слизью», 2001 г. Тел. (095) 454-7292; e-mail: E-mail: ansh@corbina.ru В аптеке: - Я надеюсь у вас есть медицинское образование? - Да, конечно. - Вы хорошо учились? - Да. - Вы давно работаете? - 20 лет. - Вы учились в провинции или в столице? - В столице. - Ну, хорошо. Тогда дайте мне, пожалуйста, пачку ваты.
|