Обоснование дифференцированного подхода к индукции овуляции.
|
Синдром поликистозных яичников (СПКЯ), являясь наиболее частой причиной ановуляторного бесплодия [1, 2], неизменно привлекает внимание ученых [3—7].
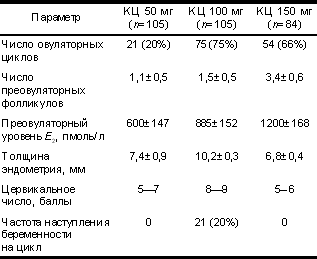
Следует признать, что на современном уровне развития науки успех лечения больных с СПКЯ связан в основном с восстановлением овуляции и достижени ем беременности у ранее бесплодных пациенток, а не с излечением этого патологического состояния [1, 8—10]. Исследования в области репродуктивной гинекологии послужили основанием для синтеза и клинического применения лекарственных препаратов, стимулирующих овуляцию и тем самым дающих возможность реализации детородной функции. В течение многих десятилетий «первой линией терапии» бесплодия при СПКЯ являлся кломифенцит рат. Но наличие кломифенрезистентных форм синдрома (30—40%, по данным разных авторов) ограничивает применение этого индуктора овуляции [8, 11]. С синтезом и использованием в клинической практике новых индукторов овуляции: менопаузаль ных гонадотропинов [12—14], рекомбинантных гонадотропинов [15—19] и аналогов ГнРГ [20—23], появилась возможность выбора метода лечения бесплодия при СПКЯ. Вместе с тем критерии адекватного выбора недостаточно полно представлены в литературе, а оценка эффективности и побочного действия индукторов овуляции подчас противоре чива. В связи с этим актуальным и важным для клинической практики является выбор наиболее адекватной в каждом конкретном случае схемы индукции овуляции. Это позволит сократить время лечения и повысить эффективность восстановления репродуктив ной функции у пациенток с СПКЯ. Целью настоящего исследования явилось определение критериев для дифференцированного назначения индукторов овуляции при лечении бесплодия у больных с СПКЯ. Материал и методы В исследование включены 130 пациенток репродуктивного возраста (в среднем 28,7±3,8 года) с СПКЯ и бесплодием. Диагноз СПКЯ установлен на основании общепринятых критериев, характеризующих этот синдром. Нарушение менструального цикла с менархе отмечалось у 100% больных, из них у 76% по типу олигоменореи. Ановуляция подтверждена тестами функциональной диагностики и определением содержания прогестерона в предполагаемую лютеиновую фазу менструального цикла. Ожирение выявлено у 68% пациенток, гирсутизм — у 57%, гиперандрогения — у 95%, повышение соотношения ЛГ/ФСГ — у 98%. Ультразвуковые признаки поликистозных яичников зарегистрированы у большинства пациенток: увеличение объема яичников — у 97%, увеличение яичниково -маточного индекса — у 80%, мелкокистозная структура яичников — у 98%, из них у 24% отмечалось периферическое расположение кистозных фолликулов. У всех больных исключены другие причины бесплодия: трубы проходимы, сперма фертильна, органических изменений в малом тазу не выявлено. В исследование не включались пациентки с выраженной надпочечниковой гиперандрогенией, нарушением функции щитовидной железы, гиперпролактинемией, гонадотропной недостаточностью гипофиза и первичной яичниковой недостаточностью. Контроль параметров фолликулогенеза осуществлялся под динамическим ультразвуковым контролем в режиме: исходный осмотр на 2—3-й дни, через 3—5 дня от начала введения индукторов овуляции, а затем с 7—8-го дня цикла ежедневно для коррекции дозы вводимых препаратов и регистрации динамики роста доминантного фолликула. С целью диагностики беременности проводили тест на содержание b-ХГ в сыворотке крови на 14-й день и УЗИ на 20—21-й после введения прегнила. Гормональное исследование проводилось при помощи радиоиммунологического метода. У 10 больных исследовали характер собственной секреции гонадотропинов и ответную реакцию гонадотропинов на введение гонадолиберина. 1. Исследование характера собственной секреции гонадотропинов. У пациенток на фоне аменореи или на 5—7-й день менструального цикла брали кровь из локтевой вены через каждые 10 мин в течение 3 ч (20—22 пробы крови). 2. Проба с ГнРГ. У пациенток брали кровь для определения исходных концентраций гонадотропинов (ЛГ, ФСГ), вводили препарат ЛГ-РГ (фирма «Ferring», Германия) в дозе 100 мкг, внутривенно. Последовательные взятия крови производили через 15, 30, 45, 60 и 120 мин. В этих порциях крови также определяли концентрацию гонадотропинов. Проба считалась положительной, если в ответ на введение ЛГ-РГ отмечали увеличение концентрации ЛГ и ФСГ не менее чем в 3 раза через 30—45 мин исследования. Для индукции овуляции использовались следующие препараты. Кломифенцитрат (КЦ; фирма «Egis Pharmaceuticals», Венгрия) назначали с 5-го по 9-й день менструального цикла (МЦ) или менструально-подобной реакции (МПР) в дозах 50—100—150 мг в день per os в течение 3 мес. Человеческие менопаузальные гонадотропины (чМГ) — хумегон (фирма «Органон», Голландия) вводили с 3—5-го дня МЦ или МПР внутримышечно один раз в день в одно и то же время суток в индивидуально подбираемых дозах (150—225 МЕ ФСГ). Рекомбинантный ФСГ (рФСГ) — препарат пурегон (фирма «Органон», Голландия) вводили с 3—5-го дня МЦ или МПР внутримышечно один раз в день в одно и то же время суток в индивидуально подбираемых дозах (100—150 МЕ). В качестве индуктора овуляции использовали препарат человеческого хорионического гонадотропина прегнил (фирма «Органон», Голландия). Агонист гонадотропин-рилизинг гормона (а-ГнРГ) препарат бусерелин (фирма "Фарм-Синтез", Россия) вводили интраназально по 2 впрыскивания 3 раза в день (доза на впрыскивание — 150 мкг; 900 мкг/сут). На первом этапе для восстановления репродуктив ной функции у больных с СПКЯ использовался КЦ. Индукция овуляции КЦ проведена у 105 пациенток. Пациенткам, резистентным к терапии КЦ, на втором этапе лечения проведена индукция овуляции препаратами гонадотропинов: препаратом рФСГ (пурегон) или чМГ (хумегон). Стимуляция овуляции препаратом рФСГ (пурегон) проведена 22 пациенткам с СПКЯ (всего 26 циклов стимуляции). В качестве группы сравнения использовались результаты лечения 33 пациенток, получавших препараты чМГ (всего проведено 37 циклов индукции овуляции). Проведена стимуляция овуляции с предваритель ной десенситизацией гипоталамо-гипофизарной системы препаратом а-ГнРГ бусерелином 31 пациентке. Методом случайного выбора пациентки были разделены на две группы: в одну группу вошли 11 пациенток, у которых десенситизация гипоталамо-гипофи зарной области проводилась в течение 1 мес, в другую — 20 больных, у которых десенситизация гипоталамо-гипофизарной области проводилась в течение 3 мес. Статистический анализ клинических и лаборатор ных данных осуществлялся с использованием программы "Статистика". Результаты и обсуждение На первом этапе работы проведена индукция овуляции КЦ у 105 из 130 пациенток исследуемой группы. Выбор такого числа пациенток обусловлен тем, что при оценке результатов предшествующего лечения больных у 25 женщин отсутствовала реакция на КЦ, назначаемый им в возрастающей дозировке. Результаты индукции овуляции представлены в табл. 1. Результаты исследования показали, что наиболее адекватной и эффективной схемой индукции овуляции КЦ при СПКЯ является назначение этого препарата в дозе 100 мг в день с 5-го по 9-й день МЦ или МПР. Схему индукции овуляции при использовании препарата в дозе 50 мг в день, по всей видимости, целесообразно рассматривать как пробную, оценивающую реакцию яичников, а при использовании КЦ в дозе 150 мг выявлен периферический антиэстроген ный эффект, препятствующий наступлению беременности. Полученные данные позволили придти к выводу о необходимости модифицирования ранее существую щей схемы применения КЦ, а именно: ограничение дозы препарата до 100 мг в сутки, мониторинг циклов индукции овуляции и продолжение лечения при адекватной ответной реакции яичника в течение не более 4 мес. Эффективность использования КЦ по результатам исследования составила 20% беременностей. Мы объяснили этот факт выбранной группой пациенток, характеризующейся длительным течением заболевания, и применением различных консервативных и оперативных методов лечения, не давших положительного эффекта. Таблица 1. Результаты индукции овуляции различными дозами КЦ у больных с СПКЯ
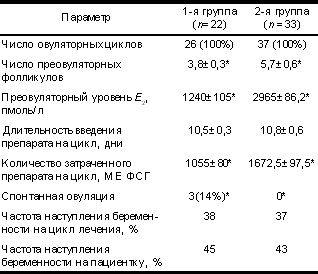
Из 130 пациенток исследуемой группы число кломифенрезистентных женщин составило 55 (25 — по данным анамнеза и 30 — после проведения первого этапа работы), что соответствовало 42% от общего числа больных. Проведено сравнение группы кломифенчувстви тельных и кломифенрезистентных женщин по клинико-лабораторным параметрам: возрасту, длительности нарушения менструального цикла, индексу массы тела (ИМТ), уровню Т, ЛГ, Е2, размерам яичников. Анализ полученных данных показал, что среди кломифенрезистентных пациенток преобладают женщины более старшего возраста, с повышенным ИМТ, высоким уровнем ЛГ, с большими размерами яичников и низким уровнем Е2. Отмечено также, что в группе кломифенрезистентных пациенток были женщины, у которых ранее беременность была достигнута при использовании КЦ, но она оказалась неразвивающейся. Этот факт может служить подтверждением того, что кломифенрезистентность, скорее всего, не является изначальным состоянием, а формируется в процессе длительного неудачного лечения бесплодия. Обобщение полученных результатов позволило сформулировать критерии, прогнозирующие кломифенрезистентность у пациенток с СПКЯ и бесплодием: — возраст > 30 лет; — ИМТ > 25; — увеличение яичников (> 40Ѕ30 мм), по данным УЗИ; — уровень ЛГ > 15 МЕ/л; — уровень Е2 < 150 пмоль/л. Если пациентка подходит по данным критериям к группе кломифенрезистентных женщин, в этих случаях, по всей видимости, следует рассматривать КЦ как препарат для пробного курса лечения, проводить тщательный мониторинг индуцированного цикла, а в случае неадекватного ответа яичников своевременно переходить к использованию прямых индукторов овуляции. На следующем этапе работы у кломифенрезистент ных пациенток проведена индукция овуляции прямыми индукторами — препаратами гонадотропного действия. Результаты индукции овуляции представлены в табл. 2. При сравнении результатов индукции овуляции по представленным в табл. 2 параметрам отмечены следующие различия: при использовании рФСГ отмечалось меньшее число преовуляторных фолликулов, ниже уровень Е2, меньшее количество затраченного препарата, и, что показательно, у 3 больных была зарегистрирована спонтанная овуляция без введения овуляторной дозы ХГ. Все это дало возможность оценить индукцию овуляции рФСГ как более физиологичную, в меньшей степени вызывающую гиперфункцию яичников. Однако эффективность индукции овуляции двумя прямыми индукторами оказалась одинаковой по частоте наступления беременности на женщину и цикл лечения. Вместе с тем зарегистрированные особенности фолликуло- и стероидогенеза при назначении рФСГ обеспечивали снижение числа осложнений индукции овуляции: синдрома гиперстимуляции яичников (СГЯ) с 33,3 до 15% по сравнению с введением чМГ, многоплодной беременности с 10 до 5% соответственно, невынашивание беременности зарегистрировано у 3 (10%) женщин 2-й группы и ни у одной из пациенток 1-й группы. Таким образом, все беременности, наступившие у пациенток 1-й группы, прогрессировали, тогда как репродуктивные потери у пациенток 2-й группы составили 10%. Таблица 2. Результаты индукции овуляции при применении рФСГ (1-я группа) и чМГ (2-я группа) у пациенток с СПКЯ
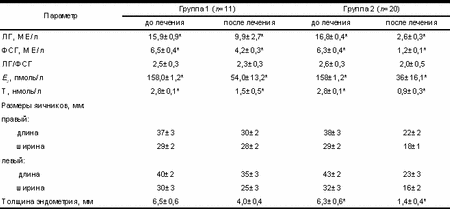
* р<0,05. Результаты настоящего исследования позволили оценить эффективность этих двух групп препаратов как одинаковую, но, учитывая особенности фолликуло генеза при использовании рФСГ, возможно рекомендовать этот препарат женщинам с СГЯ в анамнезе, а также пациенткам, относящимся к группе риска по развитию СГЯ. После проведения второго этапа исследования была выделена группа пациенток (31), у которых индукция овуляции прямыми и непрямыми индуктора ми оказалась неэффективной для восстановления репродуктивной функции. Кроме того, неэффективными оказались эндоскопические операции на яичниках, ранее проведенные у 20 из них, и методы ЭКО у 7 больных. Эти пациентки были расценены как наиболее тяжелые для реабилитации репродуктивной функции. С целью определения более эффективной схемы индукции овуляции у 10 больных этой группы проведено исследование характера собственной секреции гонадотропинов и ответная реакция гонадотропинов на введение гонадолиберина. Результаты исследования выявили наличие высокоамплитудных асинхронных выбросов ЛГ, а в ответ на введение гонадолиберина отмечается гиперергиче ская реакция ЛГ с повышением абсолютных значений до 50—70 МЕ/л. Высказано предположение, что эти патологические особенности, характеризующие гипоталамо-гипофизарные взаимоотношения при СПКЯ, затрудняют индукцию овуляции. Использование агонистов гонадолиберина для предварительной десенситизации гипоталамо-гипофи зарной области, с нашей точки зрения, является патогенетически обоснованным и, возможно, может способствовать повышению эффективности лечения бесплодия у этого контингента больных. У 11 больных а-ГнРГ применяли в течение 1 мес, а у 20 пациенток — в течение 3 мес в качестве предварительного лечения. Результаты контроля лаборатор ных параметров после использования а-ГнРГ в указанных режимах представлены в табл. 3. Зарегистрирована коррекция ранее измененных лабораторных параметров у пациенток, получавших предварительное лечение а-ГнРГ: снижение уровня ЛГ, уменьшение размеров яичников и толщины эндометрия. Однако эти параметры превышали таковые для нормальной ранней фолликулярной фазы. Лабораторные параметры после 3 мес назначения а-ГнРГ свидетельствовали о наличии выраженной десенситизации гипоталамо-гипофизарной области: снижение содержания гонадотропинов и эстрадиола до уровня гипогонадотропной аменореи, уменьшение размеров яичников. В результате индукции овуляции после месячного использования а-ГнРГ беременность была достигнута у 2 из 11 леченых пациенток, при этом в преовулятор ном периоде зарегистрированы паразитарные выбросы ЛГ (10—12 МЕ/л на 8—9-й день индуцированного цикла), которые могли, по всей видимости, явиться причиной низкой эффективности лечения. В результате 3-месячной подготовки аналогами гонадолиберина с последующей индукцией овуляции у 6 женщин наступила беременность: у 3 — в первом цикле лечения и у 3 — во втором. Эффективность лечения бесплодия составила 30 и 24% на женщину и цикл лечения соответственно. Предварительная десенситизация гипоталамо-ги пофизарной области длительным назначением агонистов гонадолиберина может явиться перспективным методом подготовки больных с СПКЯ к проведению индукции овуляции, особенно в тех случаях, когда предыдущее использование консервативных и оперативных методов лечения оказалось неэффективным для достижения беременности. Согласно результатам проведенного исследования, общая эффективность консервативного лечения бесплодия у больных с СПКЯ составила 69% беременно стей, причем среди кломифенрезистентных пациенток эффективность восстановления репродуктивной функции составила 58%. Таким образом, представленные результаты свидетельствуют о достаточно высокой эффективности консервативного лечения бесплодия при СПКЯ при условии дифференцированного применения индукторов овуляции с учетом клинико-анамнестических характеристик пациенток, результатов лабораторного обследования и анализа ответной реакции яичников. Выводы Консервативное лечение бесплодия при СПКЯ является эффективным, так как позволяет восстановить репродуктивную функцию более чем у половины больных (у 69%). Успех лечения зависит от дифференцированного назначения индукторов овуляции в зависимости от исходных характеристик больных и особенностей фолликуло- и стероидогенеза в яичниках. Около половины пациенток (42%) с СПКЯ являются кломифенрезистентными. Прогностическими критериями кломифенрезистентности могут являться старший возраст больных (больше 30 лет), ожирение с висцеральным характером распределения подкожно-жировой клетчатки, увеличенные размеры яичников с периферическим расположением кист, повы Таблица 3. Показатели исследования после применения а-ГнРГ в течение 1 (группа 1) и 3 (группа 2) мес лечения
* р < 0,05. Индукция овуляции при СПКЯ шенный уровень ЛГ (>15 МЕ/л) в сочетании с концентрацией Е2 в сыворотке крови ниже 150 пмоль/л. При использовании КЦ для индукции овуляции целесообразно ограничить дозу вводимого препарата до 100 мг в сутки, поскольку увеличение дозы до 150 мг не улучшает параметры фолликуло- и стероидогене за, приводит к выраженному периферическому антиэстрогенному эффекту и ухудшает результаты лечения бесплодия. Использование прямых индукторов овуляции (рекомбинантные и менопаузальные гонадотропины) у больных с СПКЯ одинаково эффективно — 45 и 43% беременностей соответственно, при этом применение рФСГ снижает число осложнений индукции овуляции и способствует уменьшению репродуктивных потерь. Перспективным подходом для достижения беременности при тяжелых формах СПКЯ является предварительная (в течение 3 мес) десенситизация гипоталамо-гипофизарной области, что основано на патофизиологии СПКЯ, характеризующегося наличием высокоамплитудных асинхронных выбросов ЛГ. Литература 1. Назаренко Т.А. Женское бесплодие, обусловленное нарушением процесса овуляции (клиника, диагностика, лечение): Дис. …... д-ра мед. наук. М 1998; 253. 2. Slowey M.J. Polycystic ovary syndrome: new perspective of an old problem. South Med J 2001; 94(2): 190—196. 3. Алиева Э.А. Синдром поликистозных яичников у женщин репродуктивного возраста: Дис…. ... д-ра мед. наук. М 1991; 311. 4. Гаспаров А.С. Клиника, диагностика и отдаленные результаты лечения бесплодия у пациенток с ПКЯ: Дис. ... д-ра мед. наук. М 1996; 274. 5. Lobo R.A. A disorder without identity: "HCA", "PCO", "PCOD", "PCOS", "SLS". What are we to call it?! Fertil Steril 1995; 63: 1158—1160. 6. Sills E.S., Perloe M., Palermo G.D. Correction of hyperinsulinemia in oligoovulatory women with clomiphene-resistant polycystic ovary syndrome: a review of therapeutic rationale and reproductive outcomes. Eur J Obstet Gynecol Reprod Biol 2000; 91(2): 135—141. 7. Dunaif A., Thomas A. Current concepts in the polycystic ovary syndrome. Annu Rev Med 2001; 52: 401—419. 8. Franks S. Polycystic Ovary Syndrome. New Engl J Med 1995; 13(3): 853—861. 9. Cibula D., Kuzel D. et al. Multiple ovarian biopsy in the treatment of women with polycystic ovary syndrome (PCOS). Clin Exp Obstet Gynecol 2000; 27(3—4): 194—196. 10. Здановский В.М. Современные подходы к лечению бесплодного брака: Дис. в форме научного доклада… д-ра мед. наук. М 2000; 76. 11. Gysler M. A decade's experience with an individualized clomiphene treatment. Fertil Steril 1982; 37: 161—166. 12. Baird T.D. Use of gonadotropins to induce ovulation in polycystic ovary syndrome. The ovary: Regulation, Dysfunction and Treatment. Ed. M. Filicori and C. Flamigni. 1996; 391—401. 13. Hamilton-Fairley D. Low dose gonadotropin therapy for induction of ovulation in 100 women with polycystic ovary syndrome. Hum Reprod 1991; 6: 1095—1099. 14. Buyalos R.P., Lee C.T. Polycystic ovary syndrome: pathophisiology and outcome of IVF. Fertil Steril 1996; 65(1): 1165—1178. 15. Schoot D.C., Harlin J. et al. Recombinant human follicle-stimulating hormone and ovarian response in gonadotrophin-daficient women. Hum Reprod 1994; 9: 1237—1242. 16. Out H.J., Mannaerts B.M. et al. Recombinant follicle-stimulating hormone in assisted reproduction: more oocytes, more pregnancies. Hum Reprod Update 1996; 2: 162—171. 17. Alviggi С., De Placido G. Recombinant follicle stimulating hormone is effective in poor responders to highly purified follicle stimulating hormone. Hum Reprod 2000; 15(1): 17—20. 18. Balasch J., Fabregues F. et al. Recombinant human follicle-stimulating hormone for ovulation induction in polycystic ovary syndrome: a prospective, randomised trial of two starting doses in a chronic low-dose step-up protocole. J Assist Reprod Genet 2000; 17(11): 561—565. 19. Lau E.Y., Ng E.N. et al. HMG is as good as recombinant human FSG in terms of oocyte and embryo quality: a prospective randomised trial. Hum Reprod 2001; 16(2): 319—325. 20. Смольникова В.Ю. Применение агонистов гонадотропин -рилизинг-гормона в программе ЭКО и ПЭ. Акуш и гин 1998; 1: 24—26. 21. Balen A.H., Tan S.L., MacDougall J. et al. Miscarriage rates following in vivo fertilisation are increased in women with polycystic ovaries and reduced by pituitary desensitization with buserelin. Hum Reprod 1993; 8: 959—964. 22. Fauser B., Beckers N. et al. Follicular and luteal phase characteristics following early cessation of gonadotrophin-releasing hormone agonist during ovarian stimulation in vivo fertilization. 2000; 15(1): 43—49. 23. Dor J., Bider D. et al. Effects of gonadotrophin-releasing hormone agonists on human ovarian steroid secretion in vivo and in vivo — results of a prospective, randomised in vivo fertilisation study. Hum Reprod 2000; 15(6): 1225—1230. Т.А. Назаренко, Т.Н. Чечурова, Э.Р. Дуринян, А.А. Смирнова Отделение сохранения и восстановления репродуктивной функции женщины Научного центра акушерства, гинекологии и перинатологии РАМН, Москва — Что такое здоровье? — Это когда каждый день болит в другом месте.
|