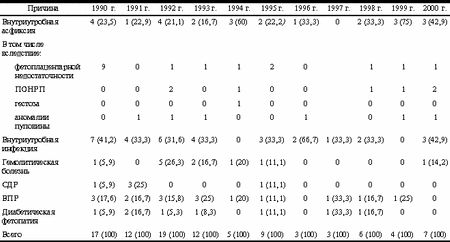
Комплексное клинико-генетическое обследование пациентов с азооспермией
|
Бесплодием страдают 10—20% супружеских пар, при этом около 40% случаев обусловлено женским фактором, около 40% — мужским, а 20% — их сочетанием. Брак считается бесплодным, если беременность не наступает в течение года регулярной половой жизни без применения противозачаточных средств (WHO, 1992). По мнению некоторых авторов, временн^ые рамки этого критерия должны составлять 6 мес.
Бесплодие у мужчин может возникнуть в результате ряда причин, наиболее частыми из которых являются воспалительные заболевания урогенитальной системы, врожденный или приобретенный гипогонадизм, варикозное расширение вен семенного канатика, крипторхизм и др. [1]. В последние годы отмечается увеличение доли бесплодия, обусловленного инфекциями, передаваемыми половым путем (гонорея, хламидиоз, микоплазмоз, вирусные инфекции и др.); часто отмечается сочетание факторов, приводящих к бесплодию. Около / случаев мужского бесплодия относят к идиопатическому [1], т.е. бесплодию с неустановленной причиной. Бульшая часть этого бесплодия, вероятно, обусловлена генетическими факторами: патологией хромосом (синдром Клайнфельтера), мутациями генов, ответственных за нарушения репродуктивной функции (синдром персистенции мюллеровых протоков, синдром Картагенера, муковисцидоз и др.) [2]. Хромосомные аберрации у пациентов с мужским бесплодием обнаруживаются примерно в 8—20% случаев [3—5]. В среднем 10—20% (от 1 до 55%) мужчин с идиопатическим бесплодием являются носителями микроделеций хромосомы Y, расположенных в локусе AZF (Azoospermia Factor), приводящих в 10—15% случаев к азооспермии, а в 5—10% случаев — к олигозооспермии тяжелой степени [6—22, 23—35]. При обследовании мужчин с неидиопатическим бесплодием AZF-микроделеции выявляются в среднем в 7,3% [6]. Локус AZF (AZF-регион) разделен на три неперекрывающиеся области: субрегион AZFa, субрегион AZFb, субрегион AZFc. В 1999 г. было высказано предположение о существовании четвертого субрегиона — AZFd, расположенного в Yq11-интервале [27], однако все STS-локусы для предполагаемого AZFd-субрегиона (sY145, sY150, sY152, sY153, sY220, sY221, sY232, sY262) уже были ранее картированы в субрегионе AZFc (интервал 6С-6Е) [22, 31]. Для каждого субрегиона определены кандидатные гены (для AZFа — ген DFFRY, для AZFb — ген RBMY, для AZFc — ген DAZ), мутации которых могут вызывать азооспермию или олигозооспермию тяжелой степени [36]. Ведется поиск генов, контролирующих определенные этапы сперматогенеза и спермиогенеза, в частности [37—41]. Выявляются корреляции между положением и размером микроделеций субрегионов AZF и степенью выраженности нарушений стадий сперматогенеза [1, 19, 21—23, 30, 36]. Частота обнаружения AZF-микроделеций у пациентов с нарушениями сперматогенеза обусловлена критериями отбора пациентов для проведения микроделеционного анализа (неустановленность причины азооспермии либо олигозооспермии тяжелой степени при исключении других причин), а также дизайном ПЦР (выбор STS-маркеров, подбор праймеров и др.). Весьма актуальной является задача создания единой схемы отбора пациентов для проведения анализа и выработки единого плана тестирования на наличие AZF-микроделеций [6]. Медико-генетическое консультирование и молекулярно-генетический анализ субрегионов AZF-локуса на наличие микроделеций особенно важно при обследовании пациентов с целью выявления риска передачи генетических нарушений перед выполнением ИКСИ. Материал и методы За период 1997—2000 гг. проведено совместное с лабораторией ДНК-диагностики Медико-генетического научного центра РАМН комплексное клинико-генетическое обследование пациентов с нарушением репродуктивной функции [42]. В ходе обследования отобраны 44 пациента с азооспермией и/или олигозооспермией неясной этиологии, у которых были исключены такие причины нарушения сперматогенеза, как обструкция семявыносящих протоков, половые инфекции, хромосомопатии и др. Возраст пациентов 20—43 года (в среднем 31 год). Обследование включало клиническое (сбор анамнеза, осмотр), спермиологическое исследования по программе ВОЗ (1992 г.), количественный кариологический анализ (ККА) незрелых половых клеток (НПК) эякулята [43]; цитогенетический анализ по лимфоцитам периферической крови (GTG-окрашивание), определение микроделеций в AZF-локусе хромосомы Y. У некоторых пациентов исследовали биоптат яичка. Спермиологический анализ. Оценивали объем эякулята, рН, вязкость, цвет, количество сперматозоидов в 1 мл и лейкоцитов в 1 мл, долю (в %) живых, мертвых, нормальных и патологических форм и варианты патологических форм сперматозоидов. Подвижность сперматозоидов оценивали по 4 категориям: а — быстрое; b — медленное; c — непоступательное движение; d — неподвижные сперматозоиды. Количественный кариологический анализ (ККА) незрелых половых клеток (НПК) эякулята [43] позволяет тотально (мультилокусно) оценить состояние сперматогенеза и выявить блок сперматогенеза на каком-либо его этапе. Важным преимуществом данного метода, по сравнению с биопсией яичка, является его неинвазивность, что предохраняет гонады от нарушения гематотестикулярного барьера и развития аутоиммунных реакций. Кроме того, мультилокусная мозаичность гистологической картины сперматогенного эпителия затрудняет общую оценку сперматогенеза, а проведенная пункционная биопсия яичка не дает адекватной оценки сперматогенеза в целом. Таким образом, ККА НПК является методом выбора при обследовании пациентов с различными видами патозооспермии и в ряде случаев является альтернативой гистологическому исследованию биоптата яичек при азооспермии и олигозооспермии тяжелой степени. Цитогенетический анализ проводили по общепринятой методике, используя GTG-окрашивание [44]. Микроделеционный анализ локусов AZF. ДНК для проведения ПЦР выделяли из лейкоцитов периферической крови с использованием протеиназы К, последующей депротеинизацией фенол-хлороформом и осаждением этанолом. Используемый набор праймеров включал в себя 3 пары Y-специфичных STSs: 1) для субрегиона AZFa (интервал 5С-5D): DYS275; 2) для субрегиона AZFb (интервал 5P-6D): DYS224; 3) для субрегиона AZFc (интервал 6E-6F): DYS249. Отрицательный контроль ДНК женщины. Положительный контроль ДНК мужчины. ПЦР проводили в 25 мл реакционной смеси, содержащей 20 нг геномной ДНК, 25 пмоль каждого праймера, 200 мкмоль dNTPs, 1 ед. Taq-полимеразы, 6 мМ MgCl и буфер 10ґPCRB, в режиме 94 °С — 45 с, 60 °С — 45 с, 72 °С — 45 с, число циклов 28. Продукты амплификации разделяли в 7% полиакриламидном геле, который содержал 0,1% этидия бромида для окрашивания ДНК. Делеция считалась достоверной, если результат повторялся в двух последующих независимых ПЦР. Гистологическое исследование биоптата яичка. Фрагменты биоптата яичка фиксировали в смеси Буэна, проводили по спиртам восходящей концентрации и заливали в парафин. Гистологические срезы после депарафинирования окрашивали гематоксилином Эрлиха, подкрашивали эозином, после чего заключали в канадский бальзам. Анализировали васкуляризацию, состояние интерстициальной ткани (клеток Лейдига), семенных канальцев (СК), мембраны СК; отмечали наличие клеток сперматогенного эпителия на разных стадиях их развития, состояние клеток Сертоли и просвета канальцев. Результаты исследования Из 44 обследованных мужчин у 5 с диагнозом первичного бесплодия и азооспермии были обнаружены AZF-микроделеции: у 3 — микроделе ция AZFс-субрегиона, у 2 — микроделеции субрегионов AZFb и AZFс. Микроделеций в AZFа-субрегионе выявлено не было. Таким образом, количество мужчин с AZF-микроделециями среди 44 обследованных пациентов составило 13,6%, а среди пациентов с азооспермией — 22,2%, что соответствует данным литературы [8, 9, 15, 21]. Для оценки сперматогенеза использовали спермиологический анализ и методику ККА НПК. В осадке эякулята у пациентов с микроделециями примерно на 200 полях зрения были обнаружены от 30 до 129 сперматозоидов (у 50—100% сперматозоидов выявлены атипия жгутика, головки или акросомы) и от 36 до 324 НПК, а также признаки частичного блока сперматогенеза на стадиях профазы мейоза I. Анализ гистопрепаратов биоптата яичка проводили у 2 из 5 пациентов с AZF-микроделециями; в некоторых СК выявлены НПК на разных стадиях развития (сперматоциты I и II). В одном случае (шифр карты 35, микроделеция субрегионов AZFb+c) большинство СК содержали только клетки Сертоли, в единичных СК были обнаружены сперматогонии (в том числе в митозе) и сперматоциты I порядка на стадиях зиготены-ранней пахитены. Многие СК имели "эмбриональный вид" из-за отсутствия люминарной зоны (просвета в СК). Клетки на стадии сперматид и сперматозоидов не обнаружены. Мембраны СК были утолщены. Отмечалась гипоплазия интерстициальной ткани. В другом случае (шифр карты 39, микроделеция субрегиона AZFc) некоторые СК содержали только клетки Сертоли, другие были гиалинизированы, в третьих были выявлены половые клетки на разных стадиях развития до сперматоцитов I в пахитене. Отмечался частичный блок сперматогенеза в митозе и мейозе, недостаточность интерстициальной ткани. При анализе состава НПК эякулята у данных пациентов выявлены 30 и 75 сперматозоидов и сперматид соответственно, что свидетельствует об информативности ККА НПК при оценке состояния сперматогенеза по эякуляту. Было подтверждено, что ККА НПК является методом выбора при обследовании бесплодных пациентов, позволяющим оценить состояние сперматогенеза, не прибегая к оперативному вмешательству. У 2 из 5 пациентов (по не зависящим от нас обстоятельствам) вначале был проведен молекулярно-генетический анализ, у одного из них выявлено отсутствие всего локуса AZF, а у другого — делеция локусов AZFb и AZFc. Затем, по рекомендации нашей лаборатории, было выполнено кариотипирование и обнаружены делеции Yq11.21-q11.23, Yq11.22®qter (кариотип 46,XY-q-(del(Y)(q11.22®ter). Эти данные свидетельствуют о необходимости этапности клинико-генетического обследования пациентов с нарушениями сперматогенеза неясной этиологии: вначале проведение анализа кариотипа, а затем — молекулярно-генетическое исследование локуса AZF хромосомы Y на наличие мутаций [4, 42]. Обсуждение Наши данные показали, что AZF-микроделе ции обнаруживают примерно у 7,3% мужчин с бесплодием; 66% микроделеций находят у пациентов с азооспермией, 28% — при олигозооспермии тяжелой степени (число сперматозоидов <5·10/мли спорадически у 6% мужчин с числом сперматозоидов >5·10/мл) [6]. Микроделеции, охватывающие весь регион AZF либо субрегионы AZFa и AZFb, AZFb и AZFс, приводят к полному отсутствию мужских половых клеток, называемому синдромом "только клетки Сертоли" (SСОS — Sertoli cell-only syndrome) или синдром клеток Сертоли I типа [19, 22, 34, 36]. Субрегион AZFa содержит ряд кандидатных генов, ответственных за возникновение азооспермии: DFFRY (USP9Y), CDY, DBY, UTY [45, 46]. При скрининг-обследовании 576 бесплодных и 96 фертильных мужчин на наличие мутаций в генах USP9Y и DBY была обнаружена 1 точковая мутация в гене USP9Y [47]. Эта мутация, возникшая de novo, представляет собой делецию четырех нуклеотидных пар в донорном сайте сплайсинга интрона 7, которая привела к пропуску экзона 8 и синтезу укороченного белка 9. Описана полная сиквенс-карта и структура генов субрегиона AZFа, а также проведен микроделеционный анализ этого субрегиона у 173 пациентов с бесплодием и нарушениями сперматогенеза [39]. У 9 пациентов были выявлены микроделеции AZFa-субрегиона: у 6 — делеция гена DBY, по 1 случаю — делеция USP9Y, делеция USP9Y и DBY и делеция DBY и UTY. Ни у одного пациента не обнаружено делеций гена UTY. У пациентов с делециями гена DBY отмечался синдром клеток Сертоли либо тяжелые нарушения сперматогенеза. Экспрессионный анализ генов субрегиона AZFа и их Х-гомологов выявил их повсеместную экспрессию, за исключением гена DBY, экспрессирующегося только в яичках. Возможно, что ген DBY играет ключевую роль в генетическом контроле сперматогенеза [39]. Кариотип и микроделеции субрегионов AZF у пациентов с делециями локуса AZF
Гены RBM1, SMCY, TSPY и EIF1AY, как считают, являются кандидатными генами субрегиона AZFb, ответственными за сперматогенез [36, 38, 40, 41, 48]. Делеции областей, содержащих какой-либо из этих генов, приводят к раннему блоку сперматогенеза на пре- и постмейотических стадиях, что показано при гистологическом исследовании яичек. У пациентов с делециями в AZFb-субрегионе (sY113-sY143) по эякуляту обычно отмечают азооспермию, но иногда может выявляться олигозооспермия тяжелой степени. Cреди субрегионов локуса AZF наиболее часто микроделеции встречаются в AZFc-субрегионе, содержащем гены, кандидатные за возникновение азооспермии: DAZ (DAZ1), SPGY (DAZ2), TTY1 и TTY2 [49, 50], составляя около 10% случаев тяжелых нарушений сперматогенеза. У пациентов с делециями в субрегионе AZFc выявлена различная степень снижения числа сперматозоидов вплоть до синдрома клеток Сертоли II типа, а также блок сперматогенеза на уровне сперматид [18, 19, 29, 30]. Повышенный уровень секреции ФСГ сочетается со сниженной продукцией АMН, секретируемого клетками Сертоли, а также аплазией семенных канальцев [19]. На гистопрепаратах биоптата яичка обнаруживаются островки сохраненного сперматогенеза. У части пациентов с делециями в субрегионе AZFc при ТЕЗА могут быть получены сперматозоиды для последующего их использования в ИКСИ, либо КРИО-ИКСИ. Выводы В последние 50 лет отмечается увеличение числа пациентов с мужским бесплодием на фоне снижения качественных показателей эякулята. Поэтому, разработка методов диагностики нарушений сперматогенеза является приоритетным направлением в проблеме бесплодия. Дифференциальная диагностика генетически обусловленного бесплодия позволяет планировать лечение пациентов и проводить медико-генетическое консультирование перед планируемым ЭКО. Перед проведением ИКСИ необходимо обязательное генетическое обследование и консультирование супружеской пары с оценкой риска передачи потомству генетических нарушений репродуктивной функции (высокий риск передачи AZF-микроделеций от отца сыну). Обследование должно включать анализ кариотипа супругов, молекулярно-генетический анализ на носительство мутаций ряда генов, таких как CF, MDD и др.; мужчин — на носительство микроделеций в локусе AZF. В связи с расширением возможностей молекулярно-генетической диагностики мутаций генов, ответственных за функционирование различных звеньев репродуктивной системы, становится актуальным вопрос о разработке алгоритма обследования бесплодных пар и обязательном медико-генетическом консультировании пациентов с нарушением репродуктивной функции. В.Б. Черных, Л.Ф. Курило, И.К. Гоголевская, Е.М. Гришина, Т.М. Сорокина, М.А. Зенкин, И.А. Матушевский, Л.М. Василенко, Л.В. Шилейко, Л.И. Лукашева, Т.Г. Цветкова, О.В. Евграфов Медико-генетический научный центр РАМН, Москва Литература 1.Diemer T., Desjardins C. Developmental and genetics disorders in spermatogenesis. Hum Reprod Update 1999; 5: 2: 120—140. 2.Курило Л.Ф. Доля генетической патологии у пациентов с нарушением развития половой системы. Сексология и андрология. Киев 1998; 4: 18—27. 3.Курило Л.Ф., Шаповал Н.В., Дубинская В.П., Шилейко Л.В., Джгаркава Н.А., Мхитарова Е.В., Коломиец О.Л. Структура хромосомной патологии среди пациентов с нарушением репродуктивной системы. Российский съезд медицинских генетиков: Тезисы докладов. М 1994; 1: 85—86. 4.Курило Л.Ф., Шилейко Л.В., Сорокина Т.М., Гришина Е.М. Структура наследственных нарушений репродуктивной системы. Вестн РАМН 2000; 5: 32—36. 5.Bourrouillou G., Dastuque N., Colombics P. Chromosome studies in 952 infertile males with a sperm count below 10 million/ml. Hum Genet 1985; 71: 366—367. 6.Simoni M. et al. Laboratory guidelines for molecular diagnosis of Y-chromosomal microdeletion. Intern J Androl 1999; 22: 292—299. 7.Kurilo L.F., Lukasheva L.I., Bartzeva O.B., Kirilova E.A., Shilejko I.V., Sorokina T.M., Mchitarova E.V., Kozlov G.I., Kalintchenko S.Yu., Evgrafov O.V. Investigation of deletions of AZF loci in infertile marriage. Abstr 2d Europ Cytogen Confer, 3—6 July, 1999, Vienna. Cytogen Cell Genet 1999; 85: 1—2: 53—54, 200. 8.Здановский В.М., Гоголевский П.А., Гоголевская И.К., Крамеров Д.А., Тогобецкий А.С., Хилькевич Л.В., Бондарев Д.А. Тестирование микроделеций на Y-хромосоме у пациентов с различными нарушениями сперматогенеза. Пробл репрод 2000; 6: 56—59. 9.Логинова Ю.А., Нагорная И.И., Шлыкова С.А., Рыбакова М.В., Чиряева О.Г., Корнилов Н.В., Кузнецова Т.В. Цитогенетиче ское исследование и микроделеционный анализ локусов AZF у пациентов с азооспермией и олигозооспермией неясного генеза перед проведением ИКСИ. Пробл репрод 2000; 5: 27—33. 10.Bonhoff A., Fischer R., Baukloh V. et al. Frequency of Y-chromosome microdeletions (Yql1.22-23) in men with reduced sperm quality requesting assisted reproduction. Adv Exp Med Biol 1997; 424: 31—35. 11.Hargreave Т.В., Chandley А.С., Ross A. et al. Y-chromosome microdeletions and male subfertility. Androl 1996; 28: Suppl: 19—21. 12.Kostiner D.R., Turek P.J., Reijo R.A. Male infertility: analisys of the markers and genes on the human Y chromosome. Hum Reprod 1998; 13: 11: 3032—3038. 13.Kremer J.A., Tuerlings J.H., Meuleman E.J. et al. Microdeletions of the Y chromosome and intracytoplasmic sperm injection: from gene to clinic. Hum Reprod 1997; 12: 687—691. 14.Krausz C., Bussani-Mastellone C., Granchi S., McElreavey K., Scarselli G., Forti G. Screening for microdeletion of Y chromosome genes in patients undergoing intracytoplasmic sperm injection. Hum Reprod 1999; 14: 7: 1717—1721. 15.Krausz C., Quintana-Murci L., Barbaux S. et al. A high Frequency of Y Chromosome Deletion in Males with nonidiopathic Infertility. J Clin Endocrinol Metab 1999; 84: 10: 3606—3612. 16.Najmabadi H., Huang V., Yen P. et al. Substantial prevalence of microdeletions of the Y-chromosome in infertile men with idiopathic azoospermia and oligozoospermia detected using a sequence-tagged site based mapping strategy. J Clin Endocrinol Metab 1996; 81: 1347—1352. 17.Nicolai M., Mastroprimiano G., Stuppia L. et al. Microdeletions of subinterval E of the Y chromosome in idiopathic oligozoospermia (abstract). J Urol 1998; 159: Suppl: 203. 18.Pryor J.L., Kent-First M., Muallem A. et al. Microdeletions in the Y chromosome of infertile men. N Engl J Med 1997; 336: 534—539. 19.Roberts К.Р. Y-chromosome deletions and male infertility: state of the art and clinical implications. J Androl 1998; 19: 255—259. 20.Simoni M., Kamischke A., Nieschlag E. Current status of the molecular diagnosis of Y-chromosomal microdeletions in the work-up of male infertility. Initiative for international quality control. Hum Reprod 1998; 13: 1748—1764. 21.Stuppia L., Gatta V., Calabrese G. et al. A quarter of men with idiopathic oligoazoospermia display chromosomal abnormalities and microdeletions of different types in interval 6 Yq11. Hum Genet 1998; 102: 566—570. 22.Vogt P.H. Human Y-chromosome deletions in Yqll and male infertility. Adv Exp Med Biol 1997; 424: 17—30. 23.Гоголевский П.А., Гоголевская И.К. Y-хромосома и мужское бесплодие (обзор литературы). Пробл репрод 1999; 5: 26—34. 24.Cooke H.J. Y chromosome and male infertility. Rev Reprod 1999; 4: 5—10. 25.Elliott D.J., Cooke H.J. The molecular genetics of male infertility. BioEssays 1999; 19: 9: 801—809. 26.Krausz C., McElreavey K. Y chromosome and male infertility. Frontiers in Biosince 1999; 4: 1—8. 27.Kent-First M., Muallem A., Schultz J. et al. Defining Regions of the Y-chromosome Responsible for Male infertility and Identification of a forth AZF Region (AZFd) by Y-chromosome Microdeletion Detection. Mol Reprod Develop 1999; 53: 27—41. 28.Kobayashi K., Mizumo K., Hida A. et al. PCR analysis of the Y chromosome long arm in azoospermic patients: evidence for a second locus required for spermatogenesis. Hum Mol Genet 1994; 3: 11: 1965—1967. 29.Nakahori Y., Kuroki Y., Komaki R. et al. The Y chromosome region essential for spermatogenesis. Harm Res 1996; 46: Suppl: 20—23. 30.Reijo R., Alagappan R.K., Patrizio P. et al. Severe oligozoospermia resulting from deletions of azoospermia factor gene on the Y chromosome. Lancet 1996; 347: 1290—1293. 31.Reijo R., Lee T.Y., Salo P. et al. Diverse spermatogenic defects in humans caused by Y chromosome deletions encompassing a novel RNA-binding protein gene. Nat Genet 1995; 10: 383—393. 32.Shinka Т., Nakahori Y. The azoospermic factor on the Y chromosome. Acta Paediat Jap 1996; 38: 399—404. 33.Vogt P., Chandley A.C., Hargreave T.B. et al. Microdeletions in the interval 6 of the Y chromosome of males with idiopathic sterility point to disruption of AZF, a human spermatogenesis gene. Hum Genet 1992; 89: 491;496. 34.Vogt P.H., Edelmann A., Hirschmann P. et al. The azoospermia factor (AZF) on the human Y chromosome in Yql1: function and analysis in spermatogenesis. Reprod Fertil Dev 1995; 7: 685;693. 35.Vogt P.H., Edelmann A., Kirsch S. et al. Human Y chromosome azoospermia factor (AZF) mapped to different subregions in Yq11. Hum Mol Genet 1996; 5: 7: 933;943. 36.Vogt P.H. Human chromosome deletions in Yql1, AZF candidate genes and male infertility: history and update. Mol Hum Reprod 1998; 4: 739;744. 37.Cooke H.J., Hargreave T., Elliott D.J. Understanding the genes involved in spermatogenesis: a progress report. Fertil Steril 1998; 69: 6: 989;995. 38.Delbridge M.L., Lingenfelter P.A., Disteche C.M., Graves J.A.M. et al. The candidate spermatogenesis gene RBMY has a homologue on the human X chromosome. Nat Genet 1999; 22: 223;224. 39.Foresta C., Ferlin A., Moro E. Deletion and expression analysis of AZFa genes on the human Y chromosome revealed a major role for DBY in male infertility. Hum Mol Genet 2000; 9: 1161;1169. 40.Ferlin A., Moro E., Garolla A., Foresta C. Human male infertility and Y chromosome deletions: role of the AZF-candidate genes DAZ, RBM and DFFRY. Hum Reprod 1999; 14: 1710;1716. 41.Ma Ê., Inglis J.D., Sharkey A. et al. A Y chromosome gene family with RNA binding protein homology: candidates for the Azoospermia factor AZF controlling human spermatogenesis. Cell 1993; 75: 1287—1295. 42.Курило Л.Ф. Схема комплексного медико-генетического обследования пациентов с мужским бесплодием неясного генеза. Российская научно-практическая конференция "Медико-генетическое консультирование в профилактике наследственных болезней", МЗ РФ, МНОМТ, МГНЦ РАМН: Тезисы докладов. М 1997; 11: 154—155. 43.Курило Л.Ф., Чеботарев Л.В., Шилейко Л.В., Остроумова Т.В., Гаева Т.Н., Мхитаров В.А. Сравнительный анализ соотношения незрелых половых клеток на разных этапах их дифференцировки в биоптате яичка и эякуляте у пациентов с азооспермией и олигозооспермией. Пробл репрод 1997; 3: 1: 80—84. 44.Захаров А.Ф., Бенюш В.А., Кулешов Н.П., Барановская Л.И. Хромосомы человека. Атлас. М: Медицина 1982; 264. 45.Jones M.H., Furlong R.A., Burkin H., Chalmers I.J., Brown G. M., Khwaja O., Affara N.A. The Drosophila developmental gene fat facets has a human homologue in Xp11.4 which escapes X-inactivation and has related sequences on Yq11.2. Hum Mol Genet 1996; 5: 1695—1701. 46.Sargent C.A., Boucher C.A., Kirsch S., Brown G., Weiss B., Trundley A., Burgoyne P., Saut N., Durand C., Levy N., Terriou P., Hargreave T., Cooke H., Mitchell M., Rappold G.A., Affara N.A. The critical region of overlap defining the AZFa male infertility interval of proximal Yq contains three transcribed sequences. J Med Genet 1999; 36: 670—677. 47.Sun C., Skaletsky H., Birren B., Devon K., Tang Z., Silber S., Oates R., Page D.C. An azoospermic man with a de novo point mutation in the Y-chromosomal gene USP9Y. Nat Genet 1999; 23: 429—432. 48.Mazeyrat S., Saut N., Mattei M.-G., Mitchell M.J. RBMY evolved on the Y chromosome from a ubiquitously transcribed X-Y identical gene. Nat Genet 1999; 22: 224—226. 49.Menke D.B., Mutter G.L., Page D.C. Expression of DAZ, an Azoospermia Factor Candidate, in Human Spermatogonia. Am J Hum Genet 1997; 60: 237—241. 50.Habermann B., Mi H.-F., Edelmann A. DAZ (deleted in azoospermia) genes encode proteins located in human late spermatids and in sperm tails. Hum Reprod 1998; 13: 363;369. 51.de Kretser D.M. The potential of intracytoplasmatic sperm injection (ICSI) to transmit genetic defects causing male infertility. Reprod Fertil Dev 1995; 7: 137—142. Гинекологи всех стран, соединяйтесь! (дополнение) Anders Bek-Pedersen _ менеджер компании K-SYSTEMS, оборудование для IVF лабораторий, Дания E-mail: abp@k-systems.dk Ефименко Анатолий Федорович, врач акушер-гинеколог efimenco@gynec.mldnet.com Пламен Тодоров _ врач акушер-гинеколог, IVF клиника, София, Болгария E-mail: robin_m_bg@yahoo.com В Интернете начал работу сайт фирмы «Солвей Фарма» на русском языке www.solvay-pharma.ru. В разделе «круглые столы online» есть тема по акушерству и гинекологии. Там же Вы можете завести свой «круглый стол» и пригласить коллег из других учреждений и городов для дискуссии. — Доктор, когда утром раздается звон будильника, мне кажется, что в меня выстрелили. — И что, вы вскакиваете? — Нет, лежу как убитый.
|